一篇详解:三阴性乳腺癌检测PD-L1蛋白表达,抗体号怎么选?要注意什么?
时间:2025-04-05 12:09:27 热度:37.1℃ 作者:网络
《中国晚期三阴性乳腺癌临床诊疗指南(2024版)》在“PD-L1阳性晚期三阴性乳腺癌(TNBC)”部分提到,相较于其他的分子分型,三阴性乳腺癌具有更高的突变负荷、更高的PD-L1表达和较多的肿瘤浸润淋巴细胞。因此,免疫检查点抑制剂逐渐成为三阴性乳腺癌的新型治疗手段。针对PD-L1表达的评估以及gBRCA突变状态的检测具有临床应用和治疗价值,参考晚期三阴性乳腺癌的治疗路径图[1]:
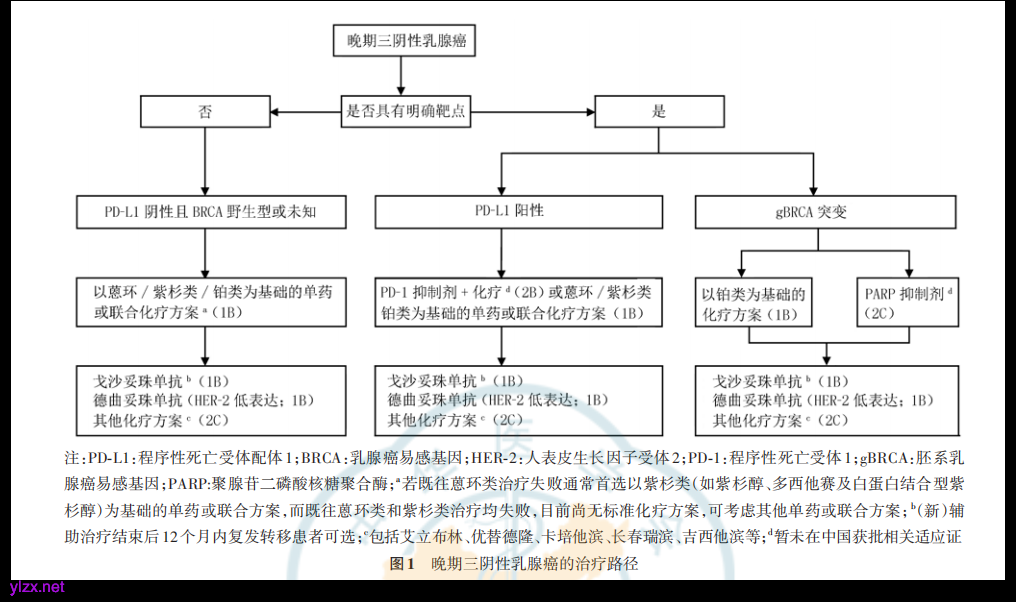
图1 摘自《中国晚期三阴性乳腺癌临床诊疗指南(2024版)》
一、PD-L1蛋白表达结果怎么解读?
针对三阴性乳腺癌,PD-L1蛋白表达结果通常有4种不同的指标结果(CPS/TPS/IC/TC),参考相关共识和研究,解释下检测结果中这些指标的含义。
肿瘤细胞阳性评分(TC、TPS)是指肿瘤细胞在任何强度下显示部分或完整膜染色的细胞数占总肿瘤细胞数的百分比,结果采用 0-100% 来表示。
免疫细胞阳性评分(IC、IPS)是指在肿瘤区域内有任何强度下染色的免疫细胞所占肿瘤面积的百分比,肿瘤面积包含肿瘤细胞、肿瘤内间质及肿瘤周围连续性相关间质,不包含坏死区域,结果采用 0-100% 来表示。
肿瘤细胞及免疫细胞综合阳性评分(CPS)是指阳性活肿瘤细胞(任何强度的部分或完全膜染色)及阳性淋巴细胞、巨噬细胞占所有活肿瘤细胞的比值,结果采用 0-100 数值来表示。

图2 指南关于PD-L1指标解释[2-3]
针对TNBC患者,我司提供22C3、JS311、SP142、28-8、SP263、E1L3N、73-10共七种抗体号,抗体克隆号的选择需结合治疗方案、药物伴随诊断要求及临床指南推荐等信息综合评估,归纳如下:
二、如何依据免疫药物选择抗体号?
帕博利珠单抗(可瑞达)——抗体号:22C3
-
适用场景及批准依据:
早期患者,基于III期临床试验KEYNOTE-522研究的数据[4],NMPA批准联合化疗新辅助治疗并在手术后继续帕博利珠单抗单药辅助治疗,用于经充分验证的检测评估肿瘤表达PD-L1(综合阳性评分CPS≥20)的早期高危三阴性乳腺癌(TNBC)患者的治疗。
晚期患者,美国FDA批准帕博利珠单抗联合化疗治疗肿瘤表达PD-L1(综合阳性评分CPS≥10)的局部复发性不可切除性或转移性TNBC患者,CSCO乳腺癌诊疗指南也同样作此推荐。
特瑞普利单抗(拓益)——抗体号:JS311
-
适用场景及批准依据:
基于TORCHLIGHT临床试验数据[5],NMPA批准特瑞普利单抗联合白蛋白结合型紫杉醇用于PD-L1阳性(综合阳性评分CPS≥1)的初治转移或复发转移性三阴性乳腺癌的治疗,CSCO乳腺癌诊疗指南也同样作此推荐。
阿替利珠单抗(泰圣奇)——抗体号:SP142
-
适用场景及批准依据:
基于IMpassion130临床研究[6],2019年,FDA加速批准了阿替利珠单抗与白蛋白结合型紫杉醇联合用于治疗PD-L1阳性(免疫细胞评分IC ≥1%)无法切除的局部晚期或转移性三阴性乳腺癌成年患者。但后来的2021年,罗氏撤回阿替利珠单抗联合白蛋白紫杉醇治疗PD-L1阳性mTNBC患者的适应症。
其他抗体号
28-8、SP263、E1L3N、73-10检测PD-L1蛋白表达在TNBC患者的指导意义,目前多处于临床研究中,可能具有准确的指导意义,但不作为优先推荐,可以关注它们与获批抗体号的一致性研究。
三、不同抗体号的一致性研究
-
TORCHLIGHT临床试验评估了JS311和22C3抗体号检测结果的一致性。在纳入的103例TNBC患者的肿瘤活检样本中,发现22C3和JS311抗体号在不同综合阳性评分CPS阈值上的总体一致性可以超过85%[5]。
-
韩国一项研究表明,三阴性乳腺癌检测PD-L1表达,在免疫细胞评分IC≥1%的临界值下,SP263与SP142抗体号检测具有可以互换的分析性能,但22C3和SP142抗体号检测则具有相似但不可互换的分析性能[7]。
-
丹娜法伯癌症中心研究表明,在转移性三阴性乳腺癌中,使用综合阳性评分CPS来检测PD-L1时,E1L3N和22C3检测方法之间的一致性超过了90%[8]。
-
MD安德森癌症中心研究表明,当以综合阳性评分CPS≥1%作为临界值时,三阴性乳腺癌PD-L1表达的阳性率在28-8检测抗体号中最高(43%),其次是22C3抗体号。并且,这两种抗体号检测在免疫细胞(IC)、肿瘤细胞(TC)和综合阳性评分(CPS)中都显示出几乎完全一致或高度一致,说明这两种检测方法的准确性较高且具有较好的一致性[9]。
四、PD-L1表达检测需要注意哪些?
-
检测方法:免疫组织化学(IHC)
-
报告周期:5个自然日
-
样本类型:
1.蜡块或防脱切片(5张),切片厚度4-5μm,适当烤片5min左右。
2.新鲜组织(手术标本/穿刺标本,福尔马林溶液保存)
3.胸腹水标本(≥30ml,无菌管保存)
-
PD-L1检测标本选择:可以参考乳腺癌CSCO指南给出的建议,对于术后复发患者,优先建议对复发和/或转移灶进行组织活检检测,若无法获取新病灶标本,可使用原发灶标本检测,具体参考如下图:

图3 乳腺癌CSCO推荐PD-L1检测标本的选择
参考文献:
[1]袁芃,徐兵河.中国晚期三阴性乳腺癌临床诊疗指南 (2024版)[J].Chinese Journal of Oncology, 2024, 46(6)DOI:10.3760/cma.j.cn112152-20240118-00034.
[2]中国抗癌协会胃癌专业委员会,梁寒,朱正纲,等.基于PD-L1蛋白表达水平的胃癌免疫治疗专家共识(2023年版)[J].中国肿瘤临床, 2024, 51(2):55-63.
[3]国家病理质控中心,中华医学会病理学分会,中国临床肿瘤学会肿瘤病理专家委员会.实体肿瘤PD-L1免疫组织化学检测专家共识(2021版)[J].中华病理学杂志, 2021, 50(7):9.DOI:10.3760/cma.j.cn112151-20210228-00172.
[4]Schmid P, Cortes J, Pusztai L, McArthur H, Kümmel S, Bergh J, Denkert C, Park YH, Hui R, Harbeck N, Takahashi M, Foukakis T, Fasching PA, Cardoso F, Untch M, Jia L, Karantza V, Zhao J, Aktan G, Dent R, O'Shaughnessy J; KEYNOTE-522 Investigators. Pembrolizumab for Early Triple-Negative Breast Cancer. N Engl J Med. 2020 Feb 27;382(9):810-821. doi: 10.1056/NEJMoa1910549. PMID: 32101663.
[5]Zhang H, Jin X, Bian L. TORCHLIGHT trial, brightening the life of more patients with advanced triple-negative breast cancer. Transl Breast Cancer Res. 2023 Sep 22;5:1. doi: 10.21037/tbcr-23-33. PMID: 38751675; PMCID: PMC11094406.
[6]Schmid P, Adams S, Rugo HS, Schneeweiss A, Barrios CH, Iwata H, Diéras V, Hegg R, Im SA, Shaw Wright G, Henschel V, Molinero L, Chui SY, Funke R, Husain A, Winer EP, Loi S, Emens LA; IMpassion130 Trial Investigators. Atezolizumab and Nab-Paclitaxel in Advanced Triple-Negative Breast Cancer. N Engl J Med. 2018 Nov 29;379(22):2108-2121. doi: 10.1056/NEJMoa1809615. Epub 2018 Oct 20. PMID: 30345906.
[7]Lee SE, Park HY, Lim SD, Han HS, Yoo YB, Kim WS. Concordance of Programmed Death-Ligand 1 Expression between SP142 and 22C3/SP263 Assays in Triple-Negative Breast Cancer. J Breast Cancer. 2020 Jun;23(3):303-313. doi: 10.4048/jbc.2020.23.e37. PMID: 32595992; PMCID: PMC7311361.
[8]Erick, Timothy K. PhD*,†; Lester, Susan C. MD, PhD‡,§;. Concordance of PD-L1 Expression in Metastatic Triple-negative Breast Cancer Between the 22C3 and E1L3N Antibodies Using Combined Positive Scoring. Applied Immunohistochemistry & Molecular Morphology 32(9):p 417-424, October 2024. | DOI: 10.1097/PAI.0000000000001223
[9]Huang X, Ding Q, Guo H, Gong Y, Zhao J, Zhao M, Sui D, Wu Y, Chen H, Liu H, Zhang J, Resetkova E, Moulder SL, Wang WL, Huo L. Comparison of three FDA-approved diagnostic immunohistochemistry assays of PD-L1 in triple-negative breast carcinoma. Hum Pathol. 2021 Feb;108:42-50. doi: 10.1016/j.humpath.2020.11.004. Epub 2020 Nov 19. PMID: 33221342.



