【协和医学杂志】CyberKnife成功治疗垂体瘤及肺癌骨转移:开启立体定向放疗新篇章
时间:2025-04-05 12:09:24 热度:37.1℃ 作者:网络
立体定向放疗已成为放疗领域的重要技术之一,可精确定位肿瘤病灶区域,使放射束在靶向病变的同时最大限度减小对周围正常组织的影响。大多数立体定向系统能将放射线准确地传送至距病灶约1 mm的位置,这种精确性使一次性施加极高辐射剂量以消灭肿瘤成为可能,从而提高临床疗效[1]。
立体定向射波手术平台简称射波刀(CyberKnife),是一项新兴的图像引导放疗技术,通过多层准直器精确塑形光束,以亚毫米级精度定位目标组织,实现高精度剂量传输[2-3]。与传统立体定向系统不同,CyberKnife对颅内和颅外肿瘤均可进行治疗[4],且在治疗过程中实时追踪图像引导,并通过机械臂自动修正偏差,从而进一步提高肿瘤照射精准度。
垂体腺瘤是常见的良性肿瘤[5],但随着疾病进展,患者可出现垂体激素功能障碍、激素过量症状或继发于视神经受压的视觉障碍等不同临床表现[6]。目前,手术切除为垂体腺瘤的标准治疗方法,但部分肿瘤邻近关键神经、血管结构,甚至延伸至垂体窝以外/侵入硬脑膜,无法完全切除,或仅采用手术切除仍存在复发风险[7]。因此,放疗成为无法手术或复发性垂体腺瘤的重要治疗选择之一。肺癌作为癌症相关死亡的主要原因之一,常发生远处器官转移。骨骼是肺癌远处转移最常见的部位之一,40%的非小细胞肺癌(NSCLC)患者可发生骨转移[8],出现骨痛、骨折、高钙血症、神经压迫等相关症状,严重影响生活质量[9]。大部分患者最终接受放疗,并实现长期肿瘤控制[10]。
本研究报道北京协和医院首次将CyberKnife技术应用于1例垂体腺瘤术后放疗后病情未得到控制的患者及1例肺腺癌靶向治疗后椎体转移患者的临床诊治过程,并详细阐述治疗疗效及随访情况,以期更全面地评估CyberKnife技术在放疗中的优势和局限性,为未来临床实践提供有益参考。
1 临床资料
1.1 患者诊疗记录
患者1
男性,53岁,2023年6月20日收入北京协和医院放疗科,主诉“12年前行垂体促甲状腺激素(TSH)大腺瘤术,接受放疗至今7年”。患者主诉2005年起出现心悸、手抖等高代谢症状。甲状腺功能检查示:TSH水平 为0.007 mIU/L(下降), 游离三碘甲状腺原氨酸(FT3)水平为12.35 pmol/L(升高), 游离甲状腺素(FT4)水平为34.85 pmol/L(升高)。
患者间断接受他巴唑治疗至2010年。2011年,外院影像学检查发现鞍区占位性病变,占位体积约2 cm×2 cm×3 cm,包绕颈内动脉,侵犯鞍底。患者接受经蝶窦垂体肿瘤切除术,病理检查结果诊断为垂体TSH腺瘤。术后心悸改善,但复查甲状腺功能未见好转。
2014年12月—2015年3月,患者共接受3次奥曲肽(善龙)20 mg肌肉注射治疗,自觉仍有手抖,但心悸症状好转。2015年6月,心悸、乏力加重,于北京协和医院行内镜下经鼻蝶窦垂体探查及鞍底重建术。术后病理结果示:角蛋白 (cytokeratin) AE1/AE3(+), 促肾上腺皮质激素(ACTH)(-), 嗜铬粒蛋白A(CgA)(+), TSH(-), 细胞核相关抗原-67 (Ki-67)(增殖指数<1%), 黄体生成素(LH)(+), 催乳素(PRL)(-), 突触素(Syn)(+),术后甲状腺功能仍未恢复。
2016年1月,行垂体残存瘤区X线调强放疗,处方剂量为45 Gy/18次。2018年8月,复查垂体增强MRI提示,垂体瘤术后改变,垂体体积减小,增强扫描可见明显强化,鞍区右侧片状低强化区,视交叉未见受压。甲状腺功能复查结果显示,TSH水平为56.65 mIU/L(升高),FT3水平为3.33 pmol/L,FT4水平为9.33 pmol/L。目前口服心得安10 mg,每8小时1次,溴隐亭3次/d,每次剂量分别为1.25 mg、1.25 mg、2.5 mg。
2023年3月,MRI动态增强扫描复查结果提示,鞍区右侧片状无明显强化区。2023年6月6日,甲状腺功能检查结果显示,TSH为1.056 mIU/L,FT3为6.71 pmol/L(升高),FT4为24.58 pmol/L(升高)。患者自觉心悸缓解,无多汗、胸痛、晕厥等症状,大便每日1次,食欲正常,体质量略增加。垂体功能检查未见皮质醇减低及生长激素缺乏。考虑患者仍存在TSH依赖性甲状腺功能亢进症,影像学检查显示鞍区仍存在局部肿瘤残留,多学科协作诊疗后建议再次放疗。
患者2
女性,62岁,2023年6月26日收住北京协和医院放疗科,主诉“左肺腺癌脑转移、纵隔淋巴结转移,并行放疗治疗,17个月后出现腰椎转移”,患者2021年4月因咳嗽发现左肺肿瘤,外院正电子发射断层显像/计算机体层成像(PET/CT)提示左肺中央型肺癌,纵隔淋巴转移(1区、2区、4~7区),病理检查结果证实为肺腺癌。脑部增强MRI显示小脑多发转移瘤。
自2021年5月起,口服泰瑞沙及贝伐珠单抗治疗。2021年5月6日—2021年5月13日,行小脑转移灶立体定向放疗,处方剂量为30 Gy/5次。2021年6月24日,脑部MRI复查结果显示,脑转移灶明显缩小,胸腹CT检查结果显示肺部病灶明显缩小。2021年12月1日,PET/CT检查结果显示左肺上叶恶性病变,伴右侧锁骨上区、左肺门、纵隔多发淋巴结转移。
2021年12月15日—2022年1月22日,行原发病灶、纵膈、锁骨上区放疗。2023年6月,CT复查结果显示,T2椎体、T12椎体以及T7椎体右侧多发高密度灶,较之前增大,考虑骨转移可能;L3椎体骨质破坏明显,高度怀疑骨转移。患者最终诊断为肺癌,伴全身多发转移及多发骨转移,L3椎体骨质破坏明显,可能影响脊柱稳定性,拟对L3椎体行转移灶放疗。
1.2 患者采用CyberKnife技术放疗情况
两例患者均经过治疗前评估、肿瘤定位、靶区勾画、计划设计后实施治疗。
1 治疗前评估:收集患者病历资料,并对其进行明确诊断。患者1诊断为垂体TSH腺瘤(已行经鼻蝶垂体腺瘤切除术,鞍区已接受放疗);患者2诊断为左肺腺癌Ⅳ期,已接受靶向治疗(包括脑转移放疗、肺门及纵隔淋巴结转移放疗、锁骨上淋巴结转移放疗)。采用卡氏功能状态量表(KPS)评价患者生活质量。患者1的KPS评分为90分,患者2为70分。
2 放疗定位:选用CT模拟定位机进行照射部位扫描定位,层厚1 mm。患者1扫描头部,患者2扫描下腹部和盆腔。扫描时注意照射范围外使用铅衣保护甲状腺、性腺等射线敏感器官。患者1采用立体定向专用热塑面网进行体位固定,患者2采用体部热塑膜进行固定,并进行体表标记。
3 靶区及危及器官勾画:参考患者MRI、CT、PET/CT等影像学检查进行靶区勾画。患者1采用头部MRI(3D T1增强序列、1 mm体素)与定位CT图像融合技术进行靶区勾画,放疗靶区确定为肿瘤总体积(GTV)(鞍区残余病变区),计划靶体积(PTV)为GTV外放1 mm,危及器官包括脑干、晶体、视交叉及视神经。患者2的临床靶体积(CTV)为L3椎体及周围高危区,PTV为CTV外放3 mm,危及器官包括脊髓、小肠及肾脏。
4 计划制定:选择CyberKnife加速器与Precision计划系统进行放疗计划的设计。放疗方式采用图像引导放疗和立体定向放疗,并分别采用颅骨追踪和脊柱追踪两种实时图像引导方式。患者1鞍区残余病变放疗的处方剂量为27 Gy/3次,其外放1 mm区域形成PTV,100%处方剂量覆盖98%的PTV,放疗危及器官剂量见表1。患者2的CTV为L3椎体及周围高危区,处方剂量为24 Gy/6次,将其外放3 mm,生成PTV,100%处方剂量覆盖95%的PTV。GTV(L3椎体转移灶)处方剂量为36 Gy/6次,将其外放3 mm,生成计划大体肿瘤区(PGTV),100%处方剂量覆盖95%的PGTV,危及器官剂量见表2。
表1 患者1放疗危及器官剂量
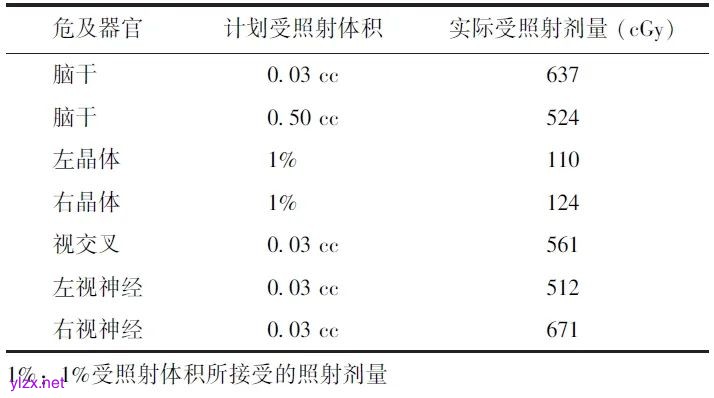
表2 患者2放疗危及器官剂量
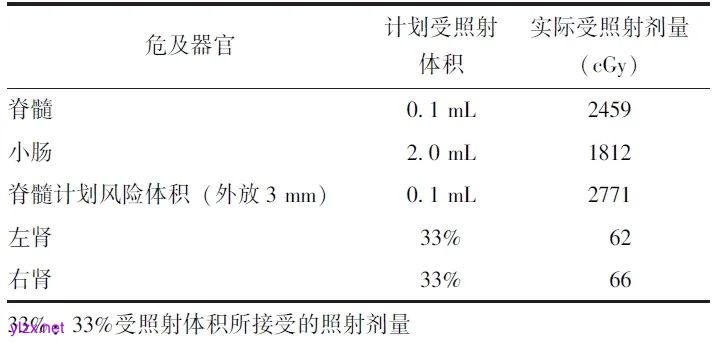
5 治疗:治疗时注意患者正确摆位,放疗期间密切观察病情变化,注意预防不良反应的发生。
1.3 CyberKnife技术与调强适形放疗计划剂量比较
两例患者CyberKnife技术与调强适形放疗计划剂量对比见图1和图2。
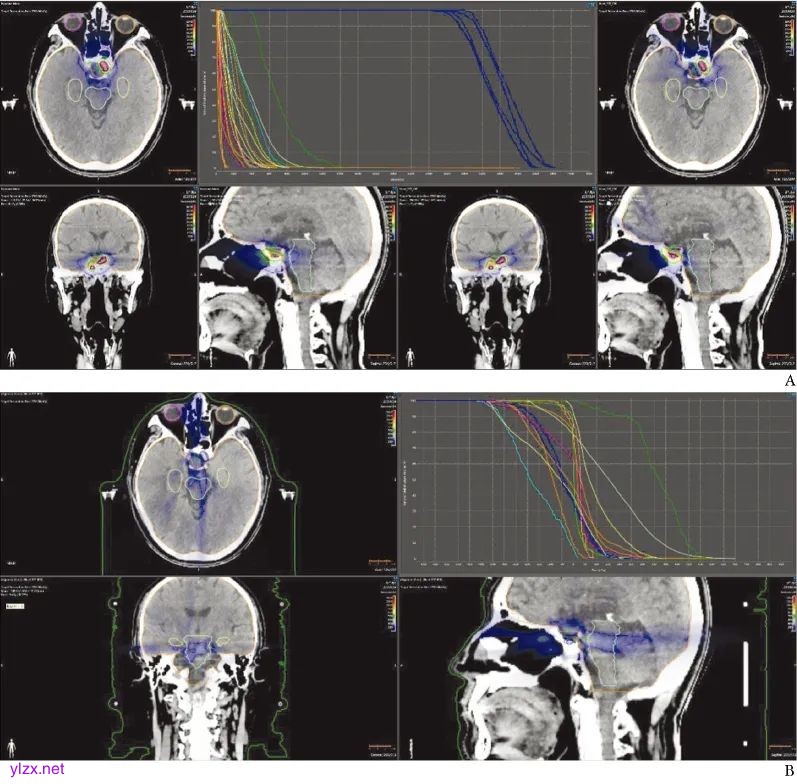
图1 患者1采用CyberKnife与普通调强适形放疗计划剂量比较
A.CyberKnife(右)与普通调强适形放疗计划(左)剂量分布;B. CyberKnife与普通调强适形放疗计划剂量差异
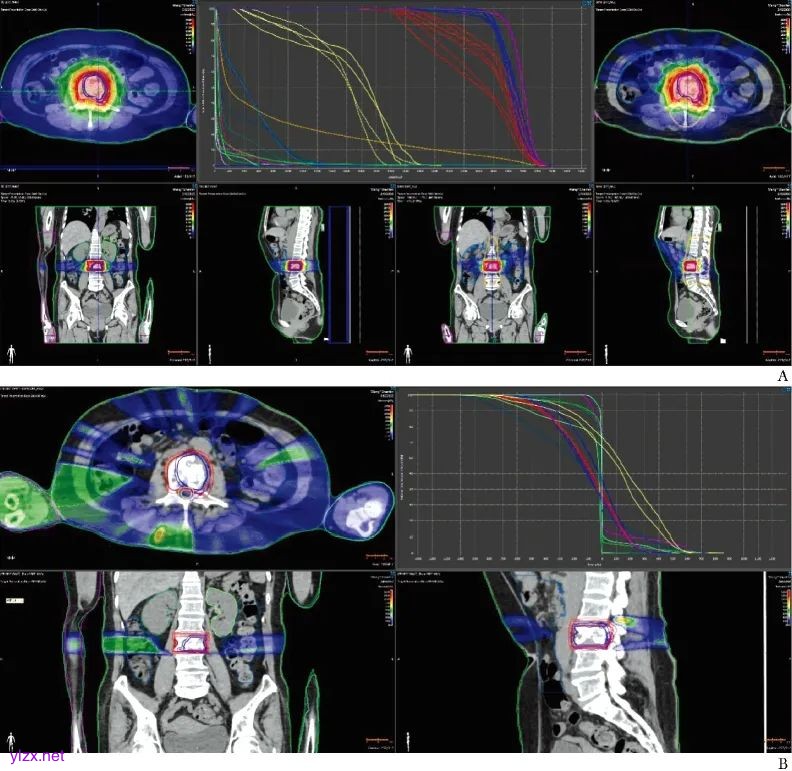
图2 患者2采用CyberKnife与普通调强适形放疗计划剂量比较
A.CyberKnife(右)与普通调强适形放疗计划(左)剂量分布; B. CyberKnife与普通调强适形放疗计划剂量差异
两种计划剂量图对比结果显示,CyberKnife技术在不扩大PTV的前提下,可提供更高剂量照射,减少危及器官照射剂量,从而最大限度地减轻组织或器官损伤,实现更加精准的肿瘤放疗,具有显著的剂量学优势。
1.4 治疗效果及随访情况
经CyberKnife治疗后,患者1未出现头晕、头痛、视力下降等不良反应,随访监测甲状腺功能逐渐恢复正常。2024年4月,甲状腺功能复查结果显示,TSH 水平为1.247 mIU/L, FT3水平为6.10 pmol/L, FT4水平为19.31 pmol/L。患者手抖、心悸症状均缓解,但仍觉乏力,无明显多汗、怕热,食欲、睡眠尚可,体质量基本保持稳定。患者2治疗后亦未出现主要放疗不良反应,患者自觉腰痛减轻。2023年9月,PET/CT复查结果提示,新见L3锥体楔形改变,锥体骨质密度不均匀增高,代谢稍高,考虑转移灶放疗后改变。
2 讨论
本文报道了北京协和医院首次应用CyberKnife进行放疗的案例,包括1例垂体腺瘤术后放疗后病情未得到控制的患者及1例肺腺癌靶向治疗后椎体转移患者。采用CyberKnife加速器与Precision计划系统进行计划设计,对患者成功实施了立体定向放疗计划,显著提升了治疗精确度,为此类患者的治疗提供了新选择。作为一种由图像引导的立体定向放疗技术,CyberKnife主要由机器人直线加速器(安装在机器人机械手臂上的紧凑型6 MV直线加速器)和图像引导硬件(包括一对正交X线源和成像面板)构成[11]。
治疗过程中,机械臂上的直线加速器向病变靶区释放多个等中心或非等中心光子束,到达患者周围球体区域节点位置时,机械臂停止,并射出放射束,使辐射剂量得以传递[12]。X线照射肿瘤靶区后,将破坏肿瘤细胞的DNA结构,使其失去活性,从而达到治疗效果。传统的立体定向系统常采用刚性框架固定体位,易引起患者体感不适且自由度受限,不适用于颅外病变治疗。此外,传统系统治疗非球形肿瘤时也会出现剂量分布显著不均匀的情况[4]。而CyberKnife克服了这些局限性,对颅内和颅外病变均可照射治疗,为立体定向放疗技术开启了新篇章。
垂体腺瘤是常见的颅内肿瘤之一,可采用多种放疗方式治疗,如通过伽马刀进行单次立体定向放射手术及通过传统直线加速器或CyberKnife进行分割放疗。治疗方式的选择通常取决于肿瘤与视神经通路的临近程度,以及是否在无显著视神经损伤风险情况下实施立体定向放疗。对于包绕或临近视神经通路的肿瘤,分割放疗能利用肿瘤组织和正常组织生物学特性的差异,通常以25~30次照射达到总量为45.0~50.4 Gy的照射剂量[13-14]。
传统直线加速器单次照射和多次照射存在不确定性,需外扩较大范围以达到预期治疗效果,因此增加了周围重要器官组织的受损风险[15]。而CyberKnife能提供适形辐射剂量,从而减小PTV外扩范围[6]。Cho等[7]应用CyberKnife对26例垂体瘤患者进行立体定向放疗,术后随访结果显示,肿瘤控制率为92.3%,且所有功能性腺瘤的激素功能均改善,仅2例患者由于肿瘤囊性增大出现视力下降。Plitt等[6]对53例距视器3 mm的垂体腺瘤患者进行了CyberKnife放疗,平均32.5个月的随访期内,肿瘤控制率为98.1%。
CyberKnife在治疗肺癌骨转移瘤方面亦展现出颅外肿瘤的治疗优势。鉴于肿瘤在呼吸时会出现移动,放疗过程中精确剂量传输往往很难实现,尤其对于周围型肿瘤而言。此类肿瘤在深吸气或呼气时移动距离为1~3 cm[16],而CyberKnife能更好地实时跟踪随呼吸移动的肿瘤,确保精确剂量传输,并使患者治疗时保持正常呼吸,极大提升了治疗舒适性[17]。Buglione等[18]对198例发生肿瘤转移的NSCLC患者进行了CyberKnife放疗,共治疗了333个病灶(包括24个骨转移灶)。中位随访18个月后,患者总生存期为29.6个月,无进展生存期为10.6个月,疗效良好。
除垂体腺瘤及肺癌骨转移瘤外,CyberKnife放疗也应用于前列腺癌[19]、肝癌[20]、黑色素瘤[21]、恶性胶质瘤[22]等多种颅内及颅外肿瘤的治疗中,并取得了较为理想的治疗效果。Borzillo等[19]应用CyberKnife对122名中低危前列腺癌患者进行了立体定向放疗,治疗剂量为(35.00~36.25)Gy/5次。研究结果表明,患者1、2、5年无病生存率分别为92.9%,92.9%和92.3%,且未出现3~4级近远期泌尿系统及直肠不良反应,表现出较好的肿瘤控制效果和较高的安全性。
有研究[22]评估了CyberKnife治疗复发性恶性胶质瘤的安全性和有效性,结果证实使用CyberKnife对复发性恶性胶质瘤进行放疗有助于进一步提升患者存活率,且不良反应发生风险较低。此外,CyberKnife在脑动静脉畸形、动静脉瘘、震颤等颅内疾病的治疗中也展现出应用潜力,具有安全性高、疗效确切等优势。
综上所述,CyberKnife作为新兴放疗技术,实现了图像引导的立体定向放疗。该技术可利用装有直线加速器的机械臂及图像引导硬件,实现精准剂量传输。相较于其他立体定向放疗技术,CyberKnife可在治疗中进行实时影像引导和追踪,精准度更高,并能有效保护正常组织,降低并发症发生风险。本院首次应用CyberKnife对两例患者成功实施了颅内和颅外肿瘤治疗,治疗过程顺利,并取得了较为理想的临床疗效,开启了本院立体定向放疗的新篇章,也为此类治疗提供了范本和宝贵的临床经验。未来,将进一步优化整个治疗流程,加深对该技术的掌握程度,并深入探索其在更多病种中的治疗前景。
参考文献
[1]Lee M, Kalani M Y S, Cheshier S, et al. Radiation therapy and CyberKnife radiosurgery in the management of craniopharyngiomas[J]. Neurosurg Focus, 2008, 24(5): E4.
[2]Kurup G. CyberKnife: a new paradigm in radiotherapy[J]. J Med Phys, 2010, 35(2): 63-64.
[3]Soman C, Alghamdi S R M, Alazemi F N M, et al. Cyberknife radiosurgery for the treatment of head and neck cancer: a systematic review[J]. Eur J Dent, 2022, 16(2): 266-273.
[4]Adler J R, Jr, Chang S D, Murphy M J, et al. The Cyberknife: a frameless robotic system for radiosurgery[J]. Stereotact Funct Neurosurg, 1997, 69(1/4 Pt 2): 124-128.
[5]Ezzat S, Asa S L, Couldwell W T, et al. The prevalence of pituitary adenomas: a systematic review[J]. Cancer, 2004, 101(3): 613-619.
[6]Plitt A R, El Ahmadieh T Y, Aoun S G, et al. Fractionated CyberKnife stereotactic radiotherapy for perioptic pituitary adenomas[J]. World Neurosurg, 2019, 126: e1359-e1364.
[7]Cho C B, Park H K, Joo W I, et al. Stereotactic radiosurgery with the CyberKnife for pituitary adenomas[J]. J Korean Neurosurg Soc, 2009, 45(3): 157-163.
[8]He Y F, Luo W Q, Liu Y J, et al. IL-20RB mediates tumoral response to osteoclastic niches and promotes bone metastasis of lung cancer[J]. J Clin Invest, 2022, 132(20): e157917.
[9]Huang X, Shi X L, Huang D H, et al. Mutational characteristics of bone metastasis of lung cancer[J]. Ann Palliat Med, 2021, 10(8): 8818-8826.
[10]Yap W K, Shih M C, Kuo C, et al. Development and validation of a nomogram for assessing survival in patients with metastatic lung cancer referred for radiotherapy for bone metastases[J]. JAMA Netw Open, 2018, 1(6): e183242.
[11]Gibbs I C, Loo B W, Jr. CyberKnife stereotactic ablative radiotherapy for lung tumors[J]. Technol Cancer Res Treat, 2010, 9(6): 589-596.
[12]Ding C X, Saw C B, Timmerman R D. Cyberknife stereotactic radiosurgery and radiation therapy treatment planning system[J]. Med Dosim, 2018, 43(2): 129-140.
[13]Kong D S, Lee J I, Lim D H, et al. The efficacy of fractionated radiotherapy and stereotactic radiosurgery for pituitary adenomas: long-term results of 125 consecutive patients treated in a single institution[J]. Cancer, 2007, 110(4): 854-860.
[14]Purdy J A. Dose to normal tissues outside the radiation therapy patient's treated volume: a review of different radiation therapy techniques[J]. Health Phys, 2008, 95(5): 666-676.
[15]Milker-Zabel S, Debus J, Thilmann C, et al. Fractionated stereotactically guided radiotherapy and radiosurgery in the treatment of functional and nonfunctional adenomas of the pituitary gland[J]. Int J Radiat Oncol Biol Phys, 2001, 50(5): 1279-1286.
[16]Seppenwoolde Y, Shirato H, Kitamura K, et al. Precise and real-time measurement of 3D tumor motion in lung due to breathing and heartbeat, measured during radiotherapy[J]. Int J Radiat Oncol Biol Phys, 2002, 53(4): 822-834.
[17]Nuyttens J J, Van De Pol M. The CyberKnife radiosurgery system for lung cancer[J]. Expert Rev Med Devices, 2012, 9(5): 465-475.
[18]Buglione M, Jereczek-Fossa B A, Bonù M L, et al. Radiosurgery and fractionated stereotactic radiotherapy in oligometastatic/oligoprogressive non-small cell lung cancer patients: results of a multi-institutional series of 198 patients treated with “curative” intent[J]. Lung Cancer, 2020, 141: 1-8.
[19]Borzillo V, Scipilliti E, Pezzulla D, et al. Stereotactic body radiotherapy with CyberKnife System for low- and intermediate-risk prostate cancer: clinical outcomes and toxicities of CyPro Trial[J]. Front Oncol, 2023, 13: 1270498.
[20]Akino Y, Shiomi H, Higashinaka N, et al. Evaluation of lung and liver tumor dose coverage treated with the CyberKnife synchrony system with consideration of measured tracking errors[J]. Anticancer Res, 2023, 43(1): 231-238.
[21]Schmelter V, Hofmann T, Schneider F, et al. Robotic CyberKnife radiosurgery for small choroidal melanomas[J]. Melanoma Res, 2022, 32(3): 192-199.
[22]De Maria L, Terzi Di Bergamo L, Conti A, et al. CyberKnife for recurrent malignant gliomas: a systematic review and meta-analysis[J]. Front Oncol, 2021, 11: 652646.


