【柳叶刀子刊】成人肿瘤患者发热性中性粒细胞减少的诊断和经验性治疗:AGIHO指南2024更新
时间:2025-03-07 12:08:49 热度:37.1℃ 作者:网络
肿瘤患者的FN
发热性中性粒细胞减少症是治疗肿瘤中的急症,需要及时和循证临床和抗微生物药物管理,还包括临床和微生物学定义的感染以及不明原因发热(FUO),实施标准操作程序(SOP)可以通过降低发热性中心粒细胞减少(FN)相关的发病率和死亡率以及继续肿瘤治疗来改善FN患者的预后。德国血液学和医学肿瘤学会(DGHO)感染性疾病工作组(AGIHO)曾于2017年发表指南,描述了成人血液肿瘤和实体瘤患者中FUO的流行病学、风险分层、诊断和治疗。
AGIHO组织血液学家、肿瘤学家、急诊和重症监护医生、药剂师、微生物学家和传染病专家,近日在《Lancet Regional Health-Europe》更新了2024版指南,讨论了成人肿瘤患者中FN的流行病学、诊断、风险分层、一线抗菌治疗、经验性抗真菌治疗和抗菌治疗持续时间等内容,并根据欧洲临床微生物学和传染病学会(ESCMID)所描述的循证推荐强度和证据质量进行了评分,旨在为临床医生提供关于治疗肿瘤患者发热性中性粒细胞减少症的循证建议。


流行病学
不明原因发热肿瘤患者的主要病原体
FN患者的治疗选择基于大型临床研究的数据,这些研究识别了FUO癌症患者中相关的微生物作为潜在病因,数据来源于肿瘤中心的本地监测,并受到抗菌药物预防(例如,氟喹诺酮类药物)的使用、多药耐药病原体的发生率以及中心内微生物的局部区域特异性(例如霉菌)的影响。
尽管在FN发作时立即开始经验性抗感染治疗至关重要,但进行全面的诊断检查以尽可能将治疗调整为针对性治疗同样重要(AIIt)。然而,单次血培养中检出的凝固酶阴性葡萄球菌(CoNS)以及其他共生皮肤病原体(例如,棒状杆菌、芽孢杆菌属、微球菌属或痤疮丙酸杆菌)应视为污染,而不应据此调整经验性抗感染治疗方案(DIII)。此外,病毒和真菌感染也可能在治疗患者中表现为FUO,并且与高死亡率相关。抗生素治疗期间症状持续超过72-96小时应特别关注真菌感染,但它们也可能更早出现,因此如果怀疑侵袭性真菌感染(IFI),应更早启动特定的诊断和抢先治疗。
即使进行最佳的诊断检查,大约半数患者仍无法确定潜在的病原体或疾病,因此仍保持经验性抗感染治疗。选择与当地流行病学相符合的最合适的经验性治疗方案至关重要。
近年来,流行病学发生了变化,从主要由革兰阳性菌引起的感染,转变为革兰阳性菌和革兰阴性菌(GNB)在血液感染(BSI)中呈均等分布,特别是在伴FN的血液肿瘤患者中。最近波兰发布的一项流行病学监测研究显示,在最初表现为FN的肿瘤患者中,与中心静脉导管(CVC)相关的BSI中,GNB的比例显著增加。在1994年至2018年的25年间,在检测到单一微生物病原体为感染原因的情况下,GNB的比例从11.9%上升到29.4%。
意大利最近一项流行病学观察研究,描述了发热血液肿瘤患者中多微生物BSI的转变,革兰氏阳性细菌和GNB合并占所有检测到的BSI的57%。
美国的一项多中心研究(BISHOP)也报告了类似结果,该研究评估了伴FN血液系统恶性肿瘤患者中经验性抗菌治疗的准确性。在343例FUO患者队列中,革兰阳性菌和革兰阴性菌(GNB)作为血液感染(BSI)的致病菌分布均衡,共鉴定出389种病原体。有趣的是,大多数BSI是由单一需氧菌株引起的(n=290),革兰阳性菌和GNB的比例相似。多重微生物感染发生在12%的病例中。在这项大型队列研究中,最常见的革兰阴性菌分离株分别是大肠杆菌(22%)、克雷伯菌属(9%)和铜绿假单胞菌(7%)。所有BSI中(当仅有一组双份血培养对这些病原体呈阳性时,根据现行临床实践,将共生皮肤菌视为污染),革兰阳性菌包括草绿色链球菌群(24%)、金黄色葡萄球菌(8%)和肠球菌属(4%)。因此,近年来,引起BSI的革兰阳性菌的流行病学本身并没有显著变化,而作为多重微生物BSI的GNB却有真正的增加。因此,强烈建议监测当地的流行病学,以调整一线经验性治疗的选择,因为有数据显示,检测到多重耐药(MDR)GNB(如MDR铜绿假单胞菌)的情况下死亡率会增加(BIIu);在使用抗菌药物预防的情况下,这一点尤为重要。
诊断
在治疗开始之前,需要对治疗期间可能诱导中性粒细胞减少的既往感染和潜伏感染进行全面评估。临床检查应重点关注肺部、皮肤和黏膜完整性(包括肛周区域)、穿刺点和CVC出口部位、鼻窦以及局部感染的临床症状(呼吸系统、胃肠道、泌尿生殖系统、神经系统)(AIII)。
青霉素过敏
对于自报青霉素或β-内酰胺类药物过敏的患者,应根据PEN-FAST标准回顾病史(AIItu)。

PEN-FAST标准能够可靠地识别低风险患者,这些患者无需进一步检测即可接受青霉素治疗。PEN-FAST评分为0的患者可以安全地接受青霉素治疗,无需进一步检测,并可去除过敏标签(delabeled)。对于PEN-FAST评分<2分的患者,可以直接进行口服阿莫西林挑战试验(BIItu),即使不进行皮肤试验也是安全的。皮肤试验通常操作繁琐,且敏感性和特异性较低(CIItu),因此使用PEN-FAST病史和/或口服激发试验进行去标签化是更优的选择。
患者可在医疗监督下口服250mg阿莫西林,持续观察60分钟,该过程也可以通过鼻胃管在危重患者中进行。对于PEN-FAST评分为2分的患者,建议转诊至有青霉素过敏反应去标签化经验的专科诊所,但青霉素过敏试验阳性的风险仍然较低(<5%)。对于PEN-FAST评分≥3分的患者,建议转诊至专业的过敏诊所(BIItu)。
发热性中性粒细胞减少症发病时的诊断程序
对于FN患者,需要迅速进行全面评估,包括临床检查、实验室检测和可能的影像学检查,但不应延迟经验性抗生素治疗(AIIr)。诊断检查的目的是排除非感染性发热的原因,确定临床感染灶和致病病原体,并评估炎症的严重程度以指导进一步的管理。如果患者出现呼吸功能不全、神经功能障碍和低血压,应立即考虑将其收治到过渡监护治疗病房或ICU。
在患者初次就诊时必须进行仔细的临床检查,并且对于住院的发热患者,至少每天重复一次(AIIu),以发现临床感染灶并指导针对常见病原体的抗感染策略。在抗感染治疗开始之前须进行血培养。如果临床条件允许,应从不同的穿刺点至少采集两套独立的血样,以优化诊断效果(AIIt)。然而与仅采集两套血培养相比,采集三套血培养的微生物检出率更高,主要是由于培养血液体积增加。
对于留置CVC的患者,应额外从CVC中抽取一对血培养(BIIr)。对于外科植入的永久性CVC(如Hickman导管或透析导管),从每个腔室中抽取血培养可提高诊断效率。一旦开始抗生素治疗,常规的后续血培养并不能提高诊断效率,因此不推荐(DIIu)。
在以下情况下必须进行后续血培养:检测到特定病原体(如金黄色葡萄球菌或念珠菌属);出现新的发热症状或临床状况恶化;临床无反应且怀疑或证实存在耐药性(AIIu)。
可以考虑进行降钙素原(PCT)检测以评估血液感染(BSI)的可能性(BIIu),并可用于指导初始抗生素治疗。
多重PCR方法和二代测序(NGS)可能改善病原体检测的周转时间以及敏感性和特异性,尤其是在持续FUO或已接受抗感染治疗的患者中。然而这些技术在多重微生物感染中的表现可能受限,因为细菌定植可能干扰特异性。此外,许多检测仅提供有限的、甚至无抗生素敏感性信息,因此无法提供最小抑菌浓度(MIC)数据;也尚未证明这些方法在降低中性粒细胞减少症肿瘤患者死亡率方面具有优势。到目前为止,这些方法尚未取代标准微生物学诊断检测(CIIu)。代谢物分析用于预测BSI和败血症的可能性是一个有趣的概念,但尚未在临床实践中应用(DIIu)。
对于存在产超广谱β-内酰胺酶(ESBL)定植高风险的患者,因此需要以碳青霉烯类为基础的治疗,推荐进行肛周拭子监测(BIIu)。基于临床症状,推荐进行影像学检查,例如,出现呼吸系统症状时进行低剂量胸部CT扫描,或怀疑腹部感染灶时进行腹部CT扫描(AIII)。常规胸部X光片不推荐用于中性粒细胞减少症患者,因其敏感性较低(DI)。对于持续发热的患者,PET-CT可能有助于排除感染源并协助降阶梯抗感染治疗,正如PIPPIN研究所示(CIIu)。
在患有肺炎的患者中,支气管镜检查(FB)具有较高作用。抗感染治疗很少受到FB和支气管肺泡灌洗(BAL)结果的影响,主要是在单纯疱疹病毒(HSV)或流感相关肺炎病例中。因此对于正在接受广谱抗感染治疗的患者,是否需要进行FB和BAL必须谨慎权衡。然而对于怀疑IFI的患者,尽管BAL的敏感性较低,但仍是强制性的,可提高诊断的可靠性(AI)。对于在发热性中性粒细胞减少症发作时出现肺部浸润的患者,其初始治疗见于肺部浸润指南。
筛查中性粒细胞减少症高风险患者的侵袭性真菌感染
在预期中性粒细胞减少将持续超过7天的高风险患者中,建议每周两次监测半乳甘露聚糖(GM)水平,以早期发现侵袭性曲霉病(IA)(AIIr)。然而对于正在接受抗霉菌预防治疗的高风险患者,GM检测的敏感性和特异性存在担忧,因此不建议常规进行GM检测。肠外营养和哌拉西林/他唑巴坦治疗对GM水平没有影响。因此,对于未接受过抗真菌治疗的高风险患者,连续血清GM检测的价值最高。如果进行了支气管镜检和BAL,所有发热性中性粒细胞减少症患者应进行BAL液GM检查(AIIu)。
监测血清1,3-β-D-葡聚糖水平是一种替代策略,然而1,3-β-D-葡聚糖是多种致病真菌细胞壁的一部分,因此在肺孢子菌肺炎和念珠菌病中可能会升高。血清GM或1,3-β-D-葡聚糖水平不能替代侵袭性曲霉病(IA)的临床、内窥镜和培养基微生物诊断。怀疑IA的情况下,可通过结合低剂量CT扫描、CT血管造影或CT引导的肺穿刺活检,或支气管镜检查(有或没有对可疑病变进行活检)来促进诊断。对于发热发作48小时后的患者,一项小型试验研究显示,CT血管造影中缺乏血管闭塞征(VOS)对侵袭性真菌病有很高的阴性预测价值(CIIu),但还需要进行前瞻性多中心试验来证明该干预措施的益处。如果得到证实,这一概念可能有助于诊断正在接受霉菌预防治疗的患者。
复杂发热性中性粒细胞减少症的危险分层
中性粒细胞减少症与发病率和死亡率的增加有关,对于实体瘤患者也是如此。为了更好地预测在首次治疗周期中经常发生的FN风险,基于治疗前风险因素的FENCE评分可能有助于优化G-CSF的处方、预防性抗生素的使用以及患者监测的强度(BIIu)。
C反应蛋白(CRP)、降钙素原(PCT)或白细胞介素-6(IL-6)等炎症参数广泛用于预测FN的复杂病程。对于预测FN患者的BSI,PCT的检测表现优于CRP,具有更高的准确性(AIIu)。在一项回顾性队列研究中,中性粒细胞减少症肿瘤患者的阳性PCT可以预测ICU转诊和死亡。也可以进行连续生物标志物评估,因为其增加可能有助于早期发现BSI等感染并发症(BIIu)。然而需要注意的是,生物标志物评估的结果应在考虑患者表现、微生物培养结果以及放射学检查结果的相应临床情境中进行解释。
MASCC评分可用于对FN门诊患者的复杂病程风险进行分层。由于高风险评分(<21分)与预后不佳相关(AIIu),如BSI、ICU入院或死亡,MASCC评分也可用于FN患者的住院管理。将PCT水平与MASCC评分结合用于预测包括BSI或死亡在内的严重并发症,可以改善对高风险患者的识别(AIIu)。尽管经常被使用,但qSOFA评分不应作为FN患者败血症、死亡率和ICU转诊的筛查工具(DIIu),因其检测性能不如MASCC评分。
为了识别表面上FN稳定但仍然容易出现严重并发症的患者,学者开发了CISNE(Clinical Index of Stable Febrile Neutropenia)评分。与MASCC评分相比,CISNE评分在识别急诊科的低风险患者方面更有用(AIIu)。
一线治疗
FN的一线治疗需基于危险因素,其中中性粒细胞减少的预期持续时间尤为重要(表2和3):中性粒细胞减少的预期持续时间为>7天的患者为高风险患者(AIItr);“高风险”是指FN复杂病程的高风险。预期中性粒细胞减少持续时间≤7天且无其他临床危险因素的患者为并发症标准风险(AIItr)。


必须对高危患者进行住院治疗,该策略也适用于具有上述其他风险因素的标准风险患者。无其他危险因素的标准风险中性粒细胞减少症患者可在门诊治疗。
高风险患者的经验性抗菌药物治疗:中性粒细胞减少≤7天或中性粒细胞减少≤7天伴其他危险因素
住院后,在FN发作后应尽快开始一线抗菌治疗,并应包括针对肠杆菌科、铜绿假单胞菌、金黄色葡萄球菌和链球菌的药物(FN高风险患者一线治疗的治疗见图1和2)。在已知有多药耐药(MDR)细菌定植的情况下(耐多药金黄色葡萄球菌[MRSA]、耐万古霉素肠球菌[VRE]、扩展谱β -内酰胺酶大肠杆菌[ESBLE-E]),目前的数据不支持使用联合策略。然而对于脓毒性休克或严重感染的患者,对于耐多药菌血症高风险患者,可考虑联合治疗(CIII)。收到微生物检测结果后应重新评估治疗,并可能对所选治疗进行降级。
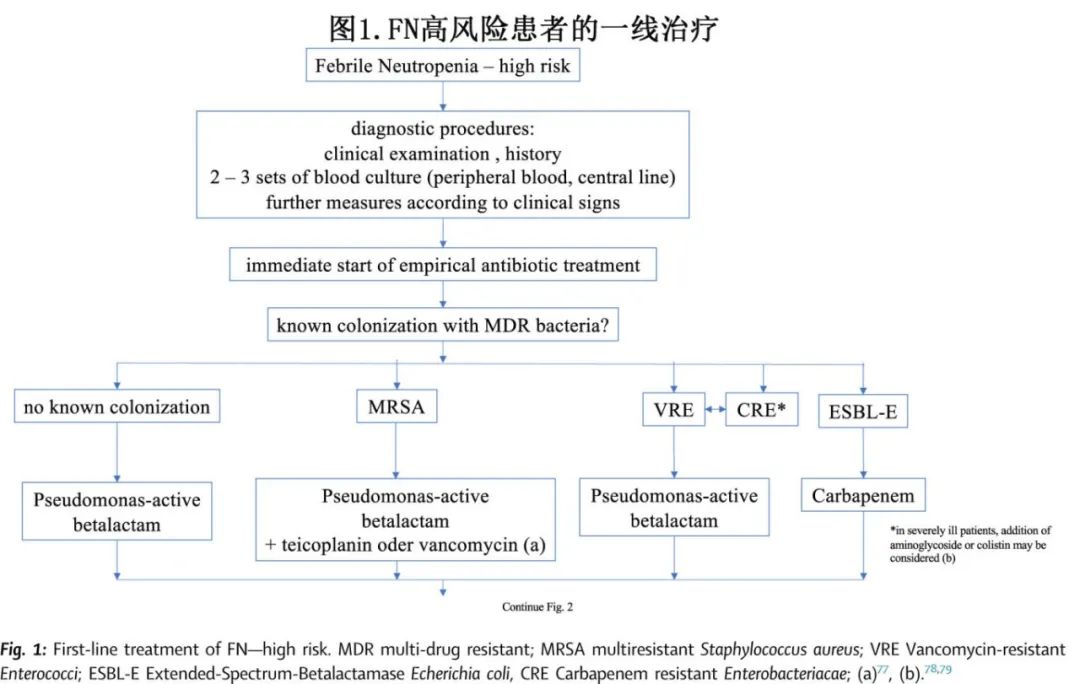
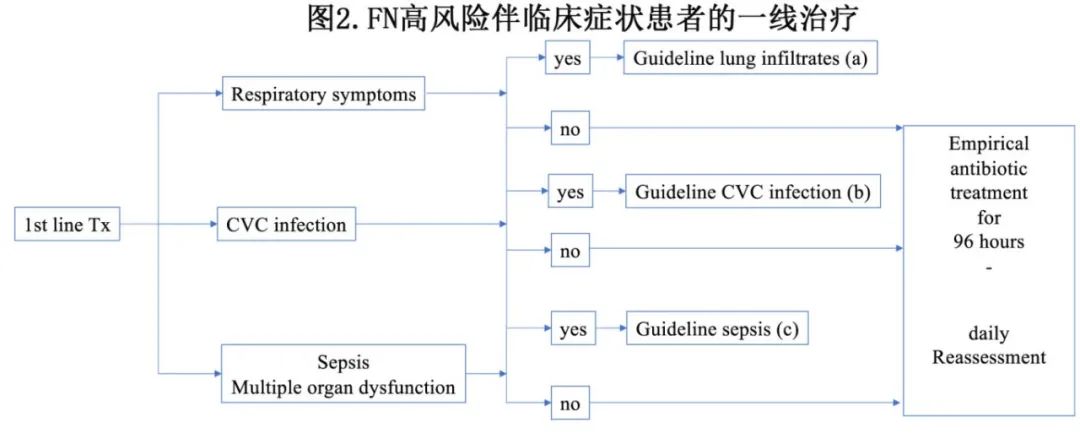
一般情况下,适合治疗FN的一线药物包括哌拉西林/他唑巴坦、亚胺培南、美罗培南和头孢吡肟。在开始发热的一线治疗时,应停止抗菌药物预防。
在FN的经验性治疗中,没有普遍使用头孢他啶/阿维巴坦等顺序抗生素(Reserve antibiotics,用于治疗多重耐药菌种的最后手段)的指征,包括头孢他啶/avibactam; 氨曲南/avibactam;ceftolozane/他唑巴坦,亚胺培南/ relebactam,美罗培南/ vaborbactam,或cefiderocol。
总之,没有普遍证据表明联合治疗在中性粒细胞减少性FUO中具有优势,经验性加入万古霉素、替考拉宁或利奈唑胺也没有显示出优越疗效。
经验性抗菌药物输注时间
在一项纳入105例FN患者的随机研究中,与标准30分钟输注相比,哌拉西林/他唑巴坦或头孢他啶延长输注4小时的总体复合反应率更高(包括发热消退、血培养转阴、临床症状和体征改善,以及无需调整抗菌药物方案)。对于有明确感染的患者,延长输注的益处是显著的,但在发热消退方面并无优势。在另一项FN患者的随机研究(n=63)中,头孢吡肟延长输注与标准输注在72小时内退热方面并无显著差异。然而,一项回顾性研究数据显示,与标准输注相比,头孢吡肟延长输注的退热时间显著缩短。因此,对于发热性中性粒细胞减少症患者,可以考虑使用延长输注时间的β-内酰胺类抗菌药物和头孢吡肟(CIII)。稳定性研究表明,持续输注不同抗菌药物是安全的。
标准风险患者的经验性一线抗菌治疗药物:中性粒细胞减少症持续时间≤7天且无其他临床风险因素
对于高风险患者适用的原则,对于无其他风险因素的标准风险患者也是强制性的:在FN发作后尽快开始抗菌治疗,并包括一种对铜绿假单胞菌有效的药物。标准风险患者如果MASCC评分较高,并且满足其他良好临床表现和完全依从性的附加标准(见表4-6),则可以考虑门诊治疗。与高风险情况不同,对于符合所有临床标准风险情况的患者,采用口服药物和门诊管理是可行的(AI)。

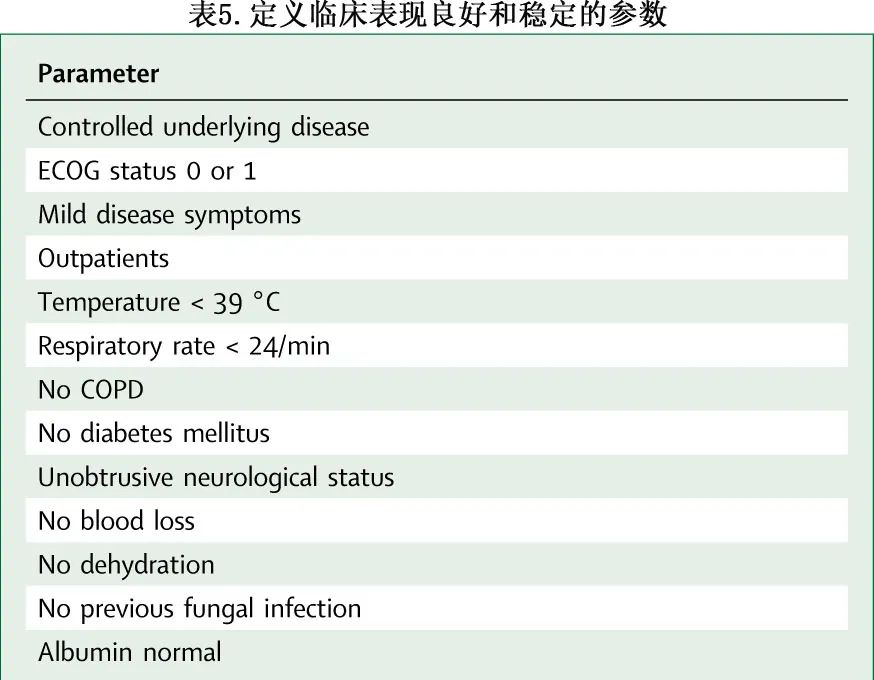

图3为标准风险FN患者的口服和门诊管理策略。
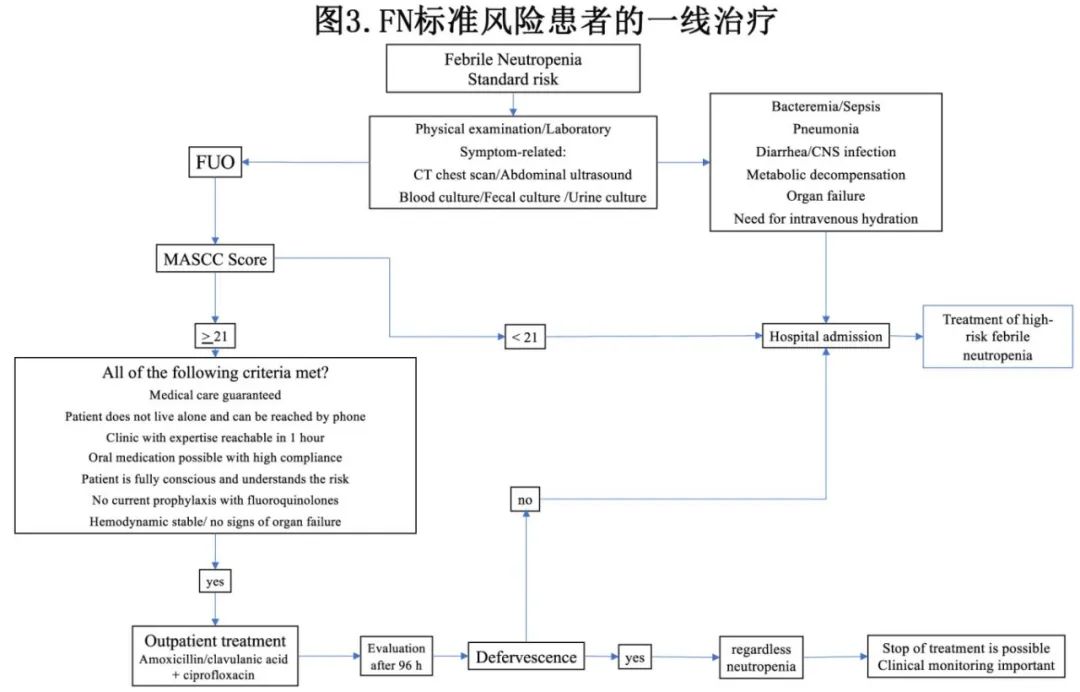
一线治疗药物包括阿莫西林/克拉维酸联合环丙沙星。莫西沙星虽然对铜绿假单胞菌无效,但在对氨苄西林或环丙沙星有禁忌的标准风险患者中可以作为替代选择。每日临床监测是强制性的。出现临床不稳定、发热未缓解或依从性丧失是立即转为住院治疗的指征。
经过初始住院和静脉启动抗菌治疗后,临床快速改善且处于标准风险的患者可以在接受2-3天有效治疗后转为门诊管理。这可能是在临床不确定情况下的一种替代方法。
临床稳定的患者应在治疗开始后观察至96小时。在接受96小时有效治疗后仍持续发热的患者应住院并重新评估,必要时调整经验性治疗方案。
在接受96小时有效治疗后退热的临床稳定患者,无论中性粒细胞是否恢复,均可停止抗菌药物治疗。近期研究表明,经验性抗菌治疗(EAT)可以在患者无发热(即体温<38℃且未使用退热药)和临床恢复后72-96小时停止,无论中性粒细胞计数如何。
二线抗生素治疗
FN患者如果出现发热复发或持续超过96小时,尤其是临床状况恶化时,应考虑调整初始经验性抗菌治疗方案。然而由于中位退热时间为3-5天,不应仅基于治疗时间长短而随意更换经验性抗菌药物(DIIr)。在两项随机对照试验中,对于哌拉西林/他唑巴坦无效或对于亚胺培南无效的的患者经验性添加万古霉素并未显示出优于安慰剂的效果,且安慰剂组45%的患者在72小时后退热。此外,在一项前瞻性研究中,对于一线抗菌药物治疗72小时后仍发热的患者经验性添加替加环素,结果显示68%的患者退热,但由于缺乏对照组且患者同时使用了其他多种抗菌药物,因此无法明确其效果。在一项回顾性研究中,未发现额外使用替加环素与未使用替加环素的患者在FN缓解方面有显著差异。因此,不推荐经验性使用替加环素。一项针对持续性发热的中性粒细胞减少症肿瘤患者的随机试验发现,亚胺培南联合糖肽类抗生素(如万古霉素或替考拉宁),以及两性霉素B去氧胆酸盐和5-氟胞嘧啶的组合,在退热方面比单独使用亚胺培南和糖肽类抗生素的挽救性抗菌治疗更有效。由于该研究缺乏适宜对照组(未改变一线抗菌治疗的对照组),因此未能明确调整经验性抗菌药物的作用。
综上所述,目前尚无研究证明在没有临床恶化和/或经临床或微生物学证实的感染的情况下,经验性更换抗生素方案优于继续使用初始抗生素。然而对于反复发热或持续发热且伴有临床恶化、不稳定或其他感染进展迹象的患者,应调整抗菌治疗。
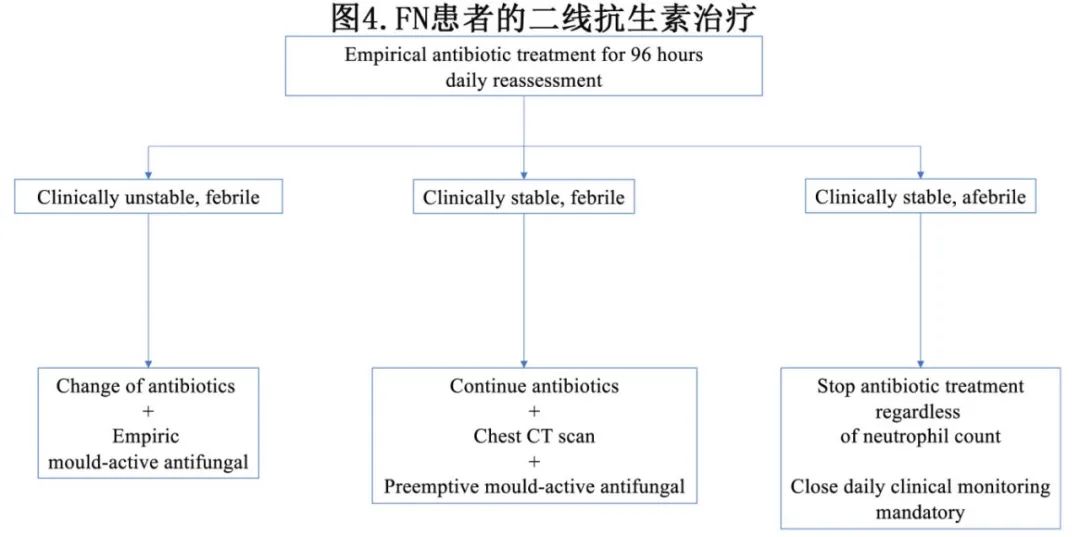
二线治疗的原则如图4所述。
经验性和抢先性抗真菌治疗
对于高风险侵袭性真菌感染(IFI)患者,如果持续发热是唯一的可疑IFI症状且对初始抗生素治疗反应不佳,可考虑经验性抗真菌治疗。而抢先性(pre-emptive)抗真菌治疗是指仅对实验室检查提示IFI或影像学高度怀疑IFI的患者使用抗真菌药物。对于特定患者群体,抢先性抗真菌治疗可以在不降低疗效的情况下减少药物毒性和治疗成本。因此,经验性治疗不如抢先性方法具有针对性。
最近的几项研究比较了抢先性治疗和经验性治疗策略。在一项随机对照试验中,对于未接受过抗真菌预防的患者,抢先性使用脂质体两性霉素B、棘白菌素或伏立康唑治疗与经验性治疗相比,在IFI发生率和死亡率方面并无劣效,但显著减少抗真菌药物的使用。在一项针对高风险中性粒细胞减少症成人的多中心随机对照试验中,抢先性治疗在使用氟康唑预防发热性中性粒细胞减少症期间,与经验性使用卡泊芬净治疗相比,在总生存率和IFI发生率方面并无劣效;正如预期,抢先性治疗组的治疗成本更低,抗真菌药物暴露时间更短。一项Cochrane系统评价纳入7项随机研究,结论是两种方法在全因死亡率和IFI相关死亡率方面无差异,但由于无法对研究参与者和人员进行盲法,证据水平较低;此外不出所料,抢先性治疗的IFI检出率更高,抗真菌药物使用更少,使用时间更短。
指南建议在高风险患者中采用抢先性抗真菌治疗,作为霉菌活性预防或经验性治疗的替代方案,前提是能够获得所需的实验室检查和影像学检查,并且检查结果能够快速反馈(BI)。大多数研究未根据本指南定义区分标准风险或高风险人群。与本指南的早期版本一样,不建议对标准风险患者使用经验性抗真菌治疗(DIII)。
一项在日本成人化疗患者中使用D指数指导米卡芬净经验性抗真菌治疗的大规模随机对照试验(RCT)表明,与标准经验性治疗相比,该方法在IFI的发生率方面具有非劣效性。D指数(累积D指数)是一个定量参数,用于评估中性粒细胞减少症的严重程度,通过计算中性粒细胞计数低于500个/μL时的累积缺陷来衡量。具体方法是绘制中性粒细胞减少期的每日中性粒细胞计数,并测量曲线下方超过500个中性粒细胞/μL线的面积。值得注意的是,该研究中患者同时包括高风险和标准风险患者,并非所有患者都接受了抗真菌预防,而接受预防的患者大多仅接受对念珠菌有效的预防。在该研究的亚组分析中,在经验性治疗环境中,米卡芬净在未接受过霉菌活性预防的患者中显示出良好的治疗效果,包括生存率在内的五项复合终点。基于中等强度的证据,推荐在高风险患者中使用D指数指导的抗真菌治疗策略(BI)。
棘白菌素类药物(尤其是卡泊芬净)在经验性治疗发热性中性粒细胞减少症方面显示出最佳的降低死亡率效果,而米卡芬净在退热方面表现出最佳的治疗反应。在另一项以退热为主要终点的回顾性研究中,卡泊芬净显示出良好的疗效,并且不良事件发生率低,无需常规监测血浆药物浓度。
在两项前瞻性RCT中,米卡芬净用于经验性治疗持续发热性中性粒细胞减少症患者,与伊曲康唑和伏立康唑相比,在退热、IFI发生率和生存率等终点方面具有非劣效性。在这两项研究中,米卡芬净的药物相关毒性较低。一项回顾性单臂研究评估了米卡芬净在脐带血移植受者中的疗效,显示出较高的退热率。艾沙康唑尚未在经验性治疗环境中与其他药物或策略进行比较。
在一项针对高风险人群的经验性治疗研究中,脂质体两性霉素B以每天1 mg/kg的剂量使用。尽管研究为非随机设计且样本量较小(n=80),但仍显示出较高疗效,且未报告IFI。在日本的一项研究中,脂质体两性霉素B以每天3 mg/kg的剂量与标准剂量200 mg静脉注射伊曲康唑(CI)进行比较,研究对象为未接受抗真菌预防的标准风险和高风险中性粒细胞减少症患者。结果显示,两组在IFI发生率、药物相关毒性和退热方面相似。
在经验性治疗环境中,两性霉素B仅应以脂质体形式使用,而其他剂型(如脂质体复合物、胶体分散剂、去氧胆酸盐)的毒性不可接受。对于接受霉菌活性抗真菌预防的患者,目前尚无前瞻性研究评估切换到另一种霉菌活性药物作为经验性治疗的疗效。
对于未接受系统性抗真菌预防的高风险患者群体,指南建议在持续发热超过72-96小时或在适当抗菌治疗后发热复发的情况下,使用霉菌活性抗真菌药物进行经验性治疗(AI)。
治疗持续时间:早期停止经验性抗生素治疗(EAT)
在一项针对709例高风险血液系统恶性肿瘤和FN患者的RCT中,相对于在中性粒细胞恢复后才停止EAT的患者,退热(即体温<38℃且未使用退热药)≥72小时且临床恢复就停止EAT的患者在无EAT天数方面显著更多(16.1天vs 13.6天)。这表明,无论中性粒细胞计数如何,EAT均可在无发热和临床恢复后72小时停止。另一项大型队列研究也发现,在稳定且至少无发热48小时的患者中,如果在72小时或更长时间后停止EAT,并不会增加感染并发症的风险;且与历史对照相比,总抗生素暴露显著减少。
相比之下,在一项RCT中,与延长碳青霉烯类应用(>9天)相比,在碳青霉烯类治疗后72小时(60-84小时)早期降阶梯治疗(无论发热是否缓解)并未导致治疗失败率增加。然而在短期治疗组,尤其是持续发热的患者中,观察到更高的严重不良事件和死亡率。几项回顾性队列研究和两项前瞻性观察研究也表明,对于无发热的中性粒细胞减少症患者,早期降阶梯EAT是可行且安全的。降钙素原(PCT)可用于指导EAT的早期停用。然而另一项研究并未显示在实施PCT指导停用时抗生素治疗天数有所减少。此外,缺乏使用PCT指导停用抗生素治疗的研究,尤其是在由于潜在其他原因(例如,基础恶性肿瘤、中性粒细胞恢复)导致持续发热的患者中。
在最近的一项RCT中,早期降阶梯和停用(early de-escalation and discontinuation,EDD)抗生素策略在细胞治疗后的发热性中性粒细胞减少症患者中也被证明是安全的。EDD组的无抗生素天数显著更少(4天 vs 6天),且不影响细胞治疗的结果。应注意的是,关于EAT的研究主要集中在血液系统恶性肿瘤患者,而关于实体瘤FN患者的数据有限。
总的来说,在退热和临床恢复后3-5天,无论中性粒细胞计数如何,均可停止EAT(AI)。这与本指南的早期版本有所不同,因为不再建议在稳定无发热开始后至少7天才停止抗菌治疗。与持续抗菌治疗直至中性粒细胞恢复相比,早期降阶梯具有更低抗生素暴露,且在临床失败率、安全性或死亡率方面无显著差异。
然而,在发热缓解后和持续中性粒细胞减少的情况下,药物干预的早期降阶梯必须伴随对患者的密切和全面临床监测,直至中性粒细胞完全恢复。对于持续中性粒细胞减少性发热的患者,密切和全面的临床监测也很重要。对于这些患者,即使培养结果阴性且临床表现稳定,也必须继续抗菌治疗。
参考文献
Sandherr M, Stemler J, Schalk E, Hattenhauer T, Hentrich M, Hertenstein B, Hohmann C, Mellinghoff SC, Mispelbaum R, Rieger C, Schmidt-Hieber M, Sprute R, Weiss G, Cornely OA, Henze L, Lass-Floerl C, Beutel G, Classen AY, Freise NF, Karthaus M, Koehler P, Krause R, Neuhann J, Orth HM, Penack O, Schaich M, Spiekermann K, Voigt S, Weissinger F, Busch E. 2024 update of the AGIHO guideline on diagnosis and empirical treatment of fever of unknown origin (FUO) in adult neutropenic patients with solid tumours and hematological malignancies. Lancet Reg Health Eur. 2025 Jan 31;51:101214. doi: 10.1016/j.lanepe.2025.101214. PMID: 39973942; PMCID: PMC11836497.


