J Immunother Cancer:PD-L1抑制剂avelumab联合/不联合西妥昔单抗治疗既往治疗过的晚期肛管鳞状细胞癌(aSCAC)患者的疗效和安全性:CARACAS研究
时间:2021-11-28 13:01:43 热度:37.1℃ 作者:网络
对于晚期肛管鳞状细胞癌(aSCAC),目前一线治疗后尚无标准治疗方法。早期的初步数据表明,表皮生长因子受体(EGFR)抑制和程序性细胞死亡配体(PD- (L))1抑制剂在既往治疗过的患者中有一定临床疗效。因此,国外学者开展了相关研究,评估PD-L1抑制剂avelumab联合/不联合西妥昔单抗治疗既往治疗过的aSCAC患者的疗效和安全性。相关结果发表在J Immunother Cancer杂志上。

这是一项开放标签、非对比,多中心随机II期试验(NCT03944252)。纳入既往经过一线或多线治疗的aSCAC患者。患者随机1:1分配至avelumab(A组)单药或联合西妥昔单抗(B)治疗。主要研究终点为客观缓解率(ORR)。在单侧α误差设为0.05,效力为80%的情况下,每组27例患者中至少有4例应答被认为是研究阳性。次要终点为无进展生存期(PFS)、总生存期(OS)和安全性。
2018年9月18日至2019年7月2日,共筛查62例患者。最终A和B组个纳入30例患者。A组24例女性(80%),B组17例女性(57%)。中位年龄63岁(范围35 - 85岁)。每组30例患者中有12例(40%)出现远处转移;A组7例(23%)和B组10例(33%)曾接受过两种或两种以上的治疗。A组有3例(10%)患者,B组有1例(3%)患者感染HIV。HPV-阳性状态在A组25例(89%)和B组26例(93%)中发现。在51例HPV-阳性患者中,HPV类型可评估的患者有36例,其中34例为HPV- 16阳性。
截止2020年9月21日,中位随访时间为17.2个月(IQR: 15.7 18.2)。A和B组中位治疗持续时间分别为3.5个月和4.6个月。A和B组的ORR 分别为10% (95% CI 2.1 to 26.5)和17% (95% CI 5.6 to 34.7);DCR分别为50% (95% CI 31.3 to 68.7)和57% (95% CI 37.4–74.5)。总共有11例患者进展后接受后续治疗,其中6例在A组,5例在B组。

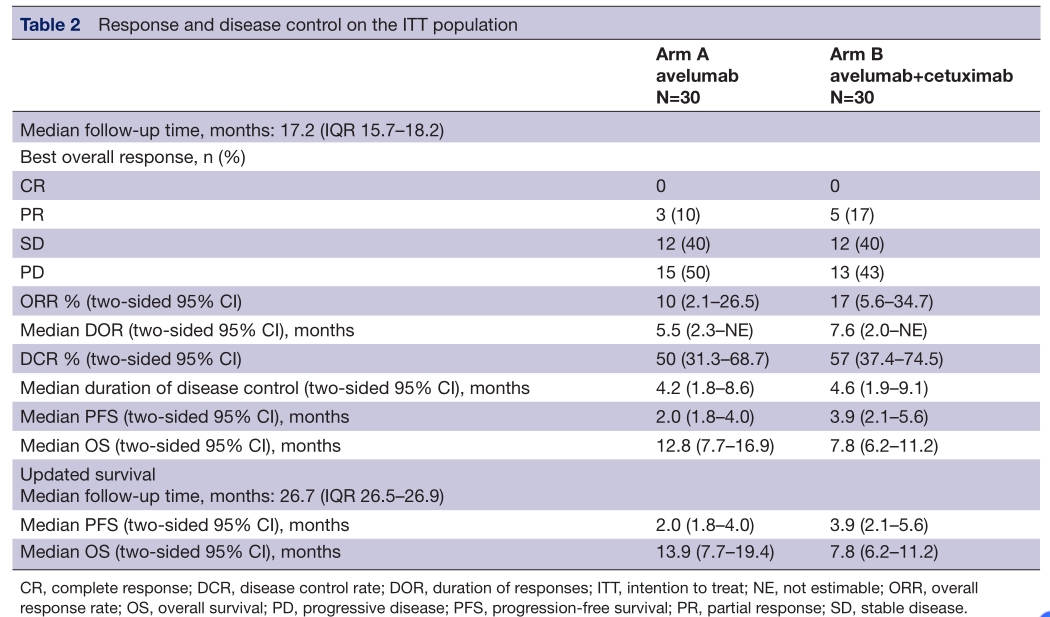
疗效评估
截止2020年9月21日,共发生55例进展和43例死亡事件。A组中位PFS (mPFS)为2.0个月(双侧95% CI 1.8 ~ 4.0), B组中位PFS为3.9个月(双侧95% CI 2.1 ~ 5.6);A组的中位OS (mOS)为12.8个月(双侧95% CI 7.7 ~ 16.9), B组为7.8个月(双侧95% CI 6.2 ~ 11.2)。
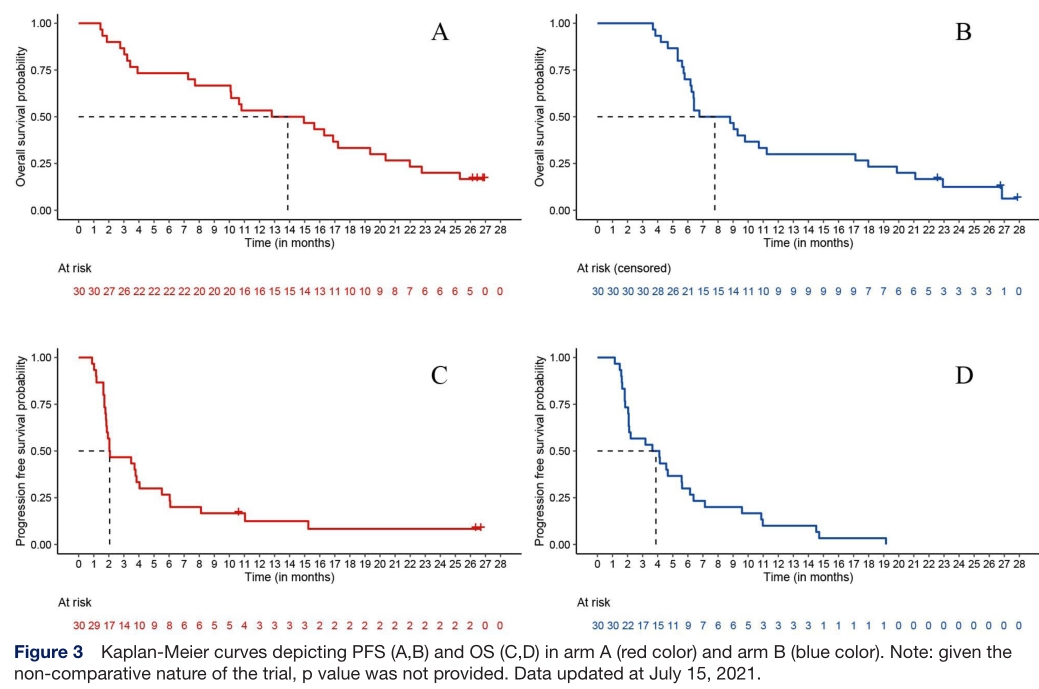
两组的PFS和OS
OS和PFS更新至2021年7月15日,中位随访时间为26.7个月( 26.5 - 26.9), 共发生56例进展和52例死亡事件。A组中位PFS (mPFS)为2.0个月(双侧95% CI 1.8 ~ 4.0), B组中位PFS为3.9个月(双侧95% CI 2.1 ~ 5.6);A组的中位OS (mOS)为13.9个月(双侧95% CI 7.7 to 19.4), B组为7.8个月(双侧95% CI 6.2 to 11.2)。
最常见的不良事件(AE)是A组的疲劳(17%)和B组的皮肤和皮下病变(87%)。A组未观察到3 - 4级治疗相关的AEs;B组中最常见的3 - 4级治疗相关AE是皮肤和皮下病变、低镁血症和天冬氨酸转氨酶/丙氨酸转氨酶升高。
综上,研究表明,CARACAS 研究在B组中达到了主要研究终点,提示在aSCAC 患者中EGFR和PD-L1双重阻断的临床疗效有一定前景。
原始出处:
Lonardi S, Prete AA, Morano F, et al. Randomized phase II trial of avelumab alone or in combination with cetuximab for patients with previously treated, locally advanced, or metastatic squamous cell anal carcinoma: the CARACAS study. Journal for ImmunoTherapy of Cancer 2021;9:e002996. doi:10.1136/ jitc-2021-002996


