Front Oncol:围手术期不同时间点CEA水平跟II期结直肠癌患者生存的关系
时间:2021-10-11 13:01:32 热度:37.1℃ 作者:网络
结直肠癌(CRC)是常见的恶性肿瘤。肿瘤复发是CRC患者不良预后的主要原因。对复发风险的预测可以优化术后辅助治疗以及随访策略来提高总体生存率。癌胚抗原(CEA)被视为CRC一个重要的预后因素,而且指南也推荐术前和术后都应该检测CEA水平。最近的研究证实术前和术后血清CEA水平都与CRC预后相关。术后CEA水平升高比术前CEA水平升高更有预后价值。因此,术后常规检测CEA水平是必要的。然而,对于II期CRC患者,术后CEA水平升高是否与预后有关仍存在争议。因此,来自国内多个医学院校开展了回顾性研究,评估围手术期不同时间点的升高的CEA水平跟II期结直肠癌患者生存的关系。相关结果发表在Frontiers in Oncology杂志上。

该研究是一项回顾性、多中心纵向队列研究,包括未接受新辅助治疗、接受根治性切除术的I - III期CRC患者。对患者进行初始和敏感性分析。获得术前1个月(CEA pre-m1)、术后1个月(CEA post-m1)、2-3个月(CEA post-m2-3)、4-6个月(CEA post-m4-6)血清CEA水平,并采用Cox回归评估其与无复发生存期(RFS)和总生存期(OS)的关系。
初步分析共纳入710例患者。710例患者中包括415名男性(58.5%),平均年龄(SD)为54.8(11.6)岁。女性患者平均年龄为54.2 ±11.2岁,男性患者平均年龄为55.3 11.8岁。腹腔镜手术385例,开放手术325例。总共699例(98.5%)患者接受了辅助化疗。中位长期随访时间为49.0个月[四分位数区间(IQR): 38.7-66.6]个月。
术前1个月(CEA pre-m1)、术后1个月(CEA post-m1)、2-3个月(CEA post-m2-3)、4-6个月(CEA post-m4-6)血清CEA水平的中位(IQR)分别为3.8(2.0-8.8)、1.8(1.2-2.9)、2.0(1.3-2.9)和2.2(1.5-3.3)ng/mL。
术前1个月(CEA pre-m1)、术后1个月(CEA post-m1)、2-3个月(CEA post-m2-3)、4-6个月(CEA post-m4-6)CEA水平升高患者的复发危险比(HR)分别为1.30 (95% CI: 0.91-1.85)、1.53 (95% CI: 0.89-2.62)、1.88 (95% CI: 1.08-3.28)和1.15 (95% CI: 0.91-1.85)。术前1个月(CEA pre-m1)、术后1个月(CEA post-m1)、2-3个月(CEA post-m2-3)、4-6个月(CEA post-m4-6)CEA水平升高患者的OS相关HRs分别为1.09 (95% CI: 0.60-1.97)、2.78 (95% CI: 1.34-5.79)、2.81 (95% CI: 1.25-6.30)和3.30 (95% CI:1.67 -.536)。
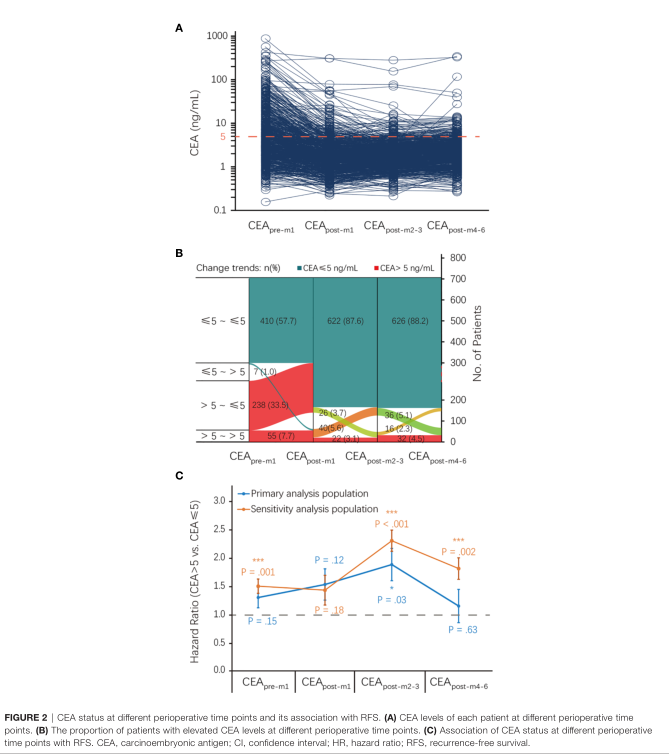
随后,经调整的多变量Cox比例风险回归分析显示,在初步分析人群中,术后2-3个月CEA升高(CEA post-m2–3),而不是其他三组,是复发的独立危险因素,但对OS则没有影响。
对比CEA正常和CEA升高的围手术期不同时间点患者的累积复发率。与CEA水平正常患者相关,术前1个月(CEA pre-m1)和术后1个月(CEA post-m1) CEA升高患者的3年复发率无显著差异,分别为19.8% vs. 15.6%和24.2% vs 16.7%。初步分析显示,术后2-3个月CEA升高的患者比术后2-3个月CEA水平正常的患者3年累积复发率更高(29.2% vs. 16.5%)。在术后4 - 6个月CEA水平升高和正常的患者之间,3年复发率没有显著差异(19.1% vs. 17.1%)。
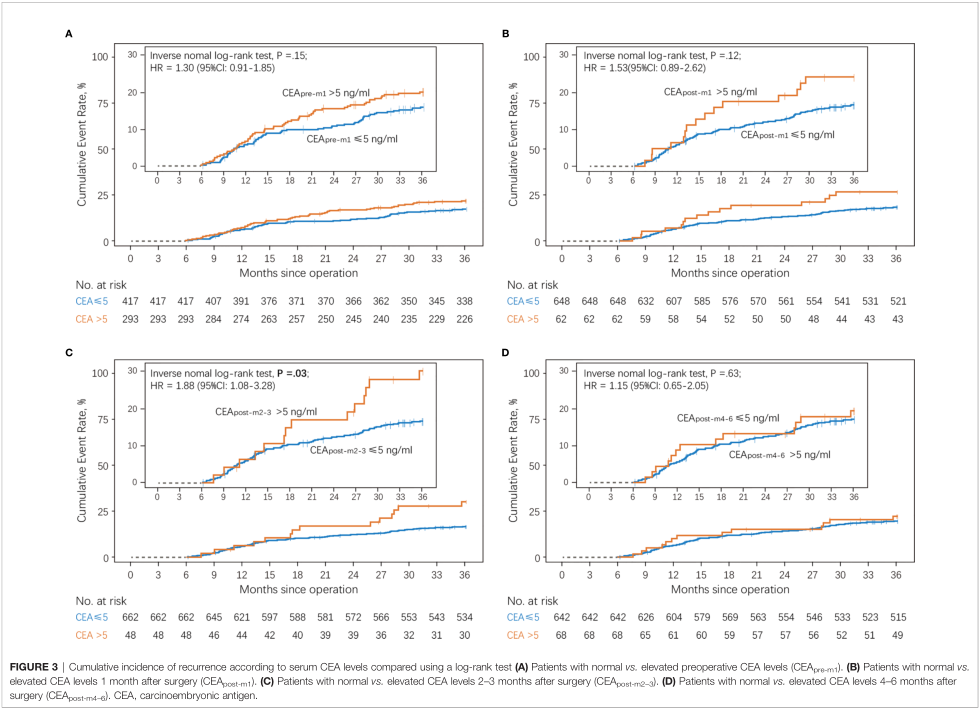
术后2-3个月CEA正常和升高患者的RFS有显著差异[n = 266; HR, 2.89; 95% CI, 1.02–8.24 (primary analysis); n = 612; HR, 2.69; 95% CI, 1.34–5.38 (sensitivity analysis)]。CEA最佳分割值为5.14 ng/mL。
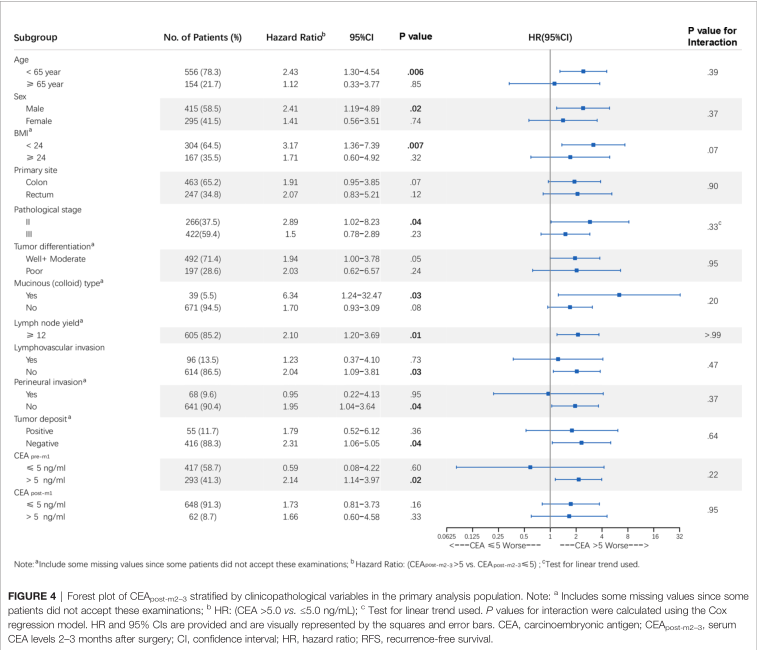
综上,研究表明,II期CRC患者术后CEA升高具有预后价值,尤其是术后2-3个月是最佳检测时间点。
原始出处:
Li Z, Zhang D, Pang X, Yan S, Lei M, Cheng X, Song Q, Cai L, Wang Z and You D (2021) Association Between Serum Carcinoembryonic Antigen Levels at Different Perioperative Time Points and Colorectal Cancer Outcomes. Front. Oncol. 11:722883.doi: 10.3389/fonc.2021.722883


