NEJM:BCMA CAR-T对来那度胺难治性多发性骨髓瘤,12个月PFS超过75%(CARTITUDE-4试验)
时间:2023-07-09 15:06:36 热度:37.1℃ 作者:网络
Ciltacabtagene autoleucel (cilta-cel) 是一种针对B细胞成熟抗原(BCMA)的CAR-T细胞疗法。在CAR-T细胞疗法中,从患者的血液中收集T细胞,并进行基因改造以表达称为嵌合抗原受体(CAR)的特殊蛋白质。CAR帮助修饰的T细胞识别并杀死癌细胞。CAR-T细胞在实验室中扩增并注入患者体内。
多发性骨髓瘤是一种无法治愈的血癌,其特征是异常浆细胞产生增加。这些浆细胞在骨髓中积聚,从而减少其他血细胞的产生。多发性骨髓瘤患者会出现骨痛、贫血、高钙血症、骨折和感染。化疗药物如阿霉素、美法仑和环磷酰胺以及皮质类固醇如地塞米松和泼尼松用于治疗多发性骨髓瘤。免疫调节药物、单克隆抗体、核输出抑制剂、蛋白酶体抑制剂等新型非化疗药物也可以用于多发性骨髓瘤患者。
2022年2月22日,美国食品药品监督管理局(FDA)批准ciltacabtagene autoleucel用于治疗复发或难治性多发性骨髓瘤患者[1]。这些患者之前必须接受过四种或更多的治疗,其中包括单克隆抗体、免疫调节药物和蛋白酶体抑制剂(三类暴露)。2023年1月2日,开发ciltacabtagene autoleucel的传奇生物宣布,该创新药物的新药申请(NDA)已获得中国国家药品监督管理局(NMPA)受理[2]。该药物已在美国和中国获得突破性疗法认定[3]。
近日,全球3期CARTITUDE-4试验结果发表在《新英格兰医学杂志》上[4]。该试验的结果也在 2023年美国临床肿瘤学会(ASCO)年会上公布了。对称为来那度胺的免疫调节药物耐药的患者参加了这项试验。这些患者之前接受过一到三种疗法。
在该试验中,患者以1:1的比例随机分配。211名患者随机接受了两种标准治疗方案中的一种。在这 211名患者中,183名患者接受了达雷妥尤单抗、泊马度胺和地塞米松(DPd),28名患者接受了泊马度胺、硼替佐米和地塞米松(PVd)。208名患者随机接受单次cilta-cel输注。
与标准治疗方案相比,Cilta-cel显著降低了死亡或疾病进展的风险。接受 cilta-cel治疗的患者未达到无进展生存期的中位持续时间。相比之下,接受标准治疗的患者的无进展生存期中位数为11.8 个月。
在12 个月时,接受cilta-cel和标准治疗方案的患者的无进展生存率(PFS)分别为75.9% 和48.6%。73.1% 接受cilta-cel治疗的患者和21.8%接受标准治疗方案的患者观察到完全缓解(CR)或更好。

cilta-cel组和标准治疗组无进展生存期的Kaplan-Meier分析
cilta-cel组中84.6%的患者和标准治疗组中67.3%的患者出现总体反应。在这项研究中,患者的总体反应意味着部分反应或更好。在对这两种方案有反应的患者中,84.7%接受cilta-cel的患者和63.0%接受标准治疗方案的患者表现出至少12 个月的反应。
01 全球新型治疗剂的疗效较低
在DREAMM-2临床试验中,难治性或复发性多发性骨髓瘤患者每三周给予3.4 mg/kg或2.5 mg/kg belantamab mafodotin[5]。Belantamab mafodotin 是一种抗体药物偶联物,针对成熟B淋巴细胞和浆细胞上的B 细胞成熟抗原(BCMA)。接受 2.5 mg/kg belantamab mafodotin 治疗的患者中有31%获得总体反应。同样,接受 3.4 mg/kg belantamab mafodotin 治疗的患者中有34%获得了总体反应。
接受2.5 mg/kg belantamab mafodotin患者中位无进展生存期为2.9个月和接受3.4 mg/kg belantamab mafodotin患者中位无进展生存期为4.9个月。13个月的长期随访报告显示,接受2.5 mg/kg belantamab mafodotin 治疗的患者中有32%达到总体反应,2.5 mg/kg 组的中位无进展生存期为2.8 个月[6]。
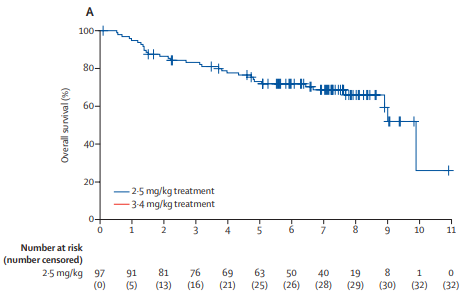
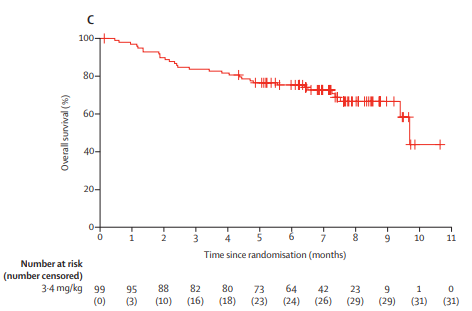
2.5 mg/kg 和3.4 mg/kg组的总生存率
在STORM临床试验中,122名难治性多发性骨髓瘤患者每周两次口服塞利尼索和地塞米松[7]。塞利尼索是一种口服抗癌剂,可抑制称为Exportin 1 (XPO1) 的核输出蛋白。大约 26%的患者出现部分缓解或更好。接受该治疗的患者的中位总生存期和中位无进展生存期分别为8.6 个月和3.7 个月。
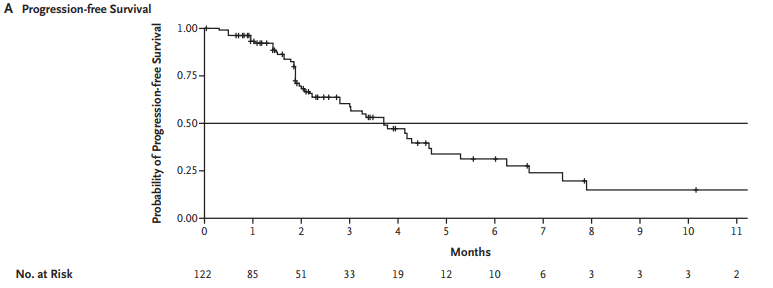

接受口服塞利尼索治疗的患者的无进展生存期和总生存期
在KarMMa临床试验中,128名对免疫调节剂、蛋白酶体抑制剂和抗CD38抗体没有反应的多发性骨髓瘤患者接受了Idecabtagene Vicleucel,这是一种CAR-T细胞疗法[8]。当患者在 13.3个月时进行随访时,大约33%的患者出现完全缓解或更好。接受 Idecabtagene Vicleucel 治疗的患者的中位总生存期和中位无进展生存期分别为19.4 个月和8.8 个月。

接受Idecabtagene Vicleucel 治疗的患者的总生存期
02 cilta-cel与医生选择的治疗的比较
将CARTITUDE-1临床试验中接受cilta-cel的患者与来自三项临床试验的患者进行比较,这些患者在停止达雷妥尤单抗联合治疗后接受医生选择的治疗[9]。医生选择的治疗组中的患者接受卡非佐米、泊马度胺、硼替佐米、来那度胺、沙利度胺和其他药物的单药治疗或联合治疗。
与医生选择的治疗方法相比,Cilta-cel实现完全缓解或更好和总体反应的可能性分别提高了111.70 倍和2.95 倍。接受医生选择的治疗的患者的中位总生存期为 10.9个月,而接受cilta-cel的患者未达到总生存期。接受 cilta-cel和医生选择的治疗的患者的中位无进展生存期分别为22.8 个月和5.6 个月。
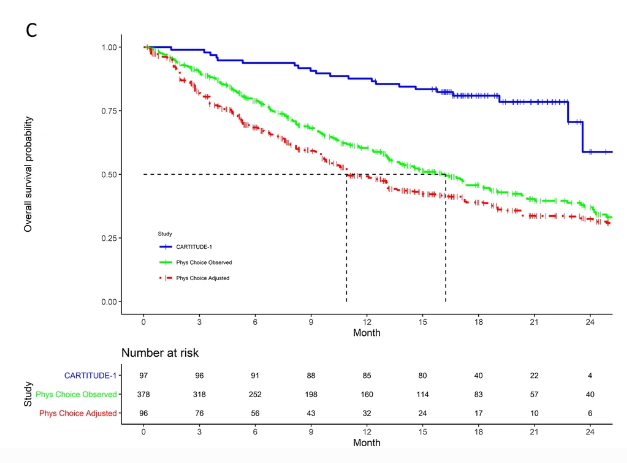
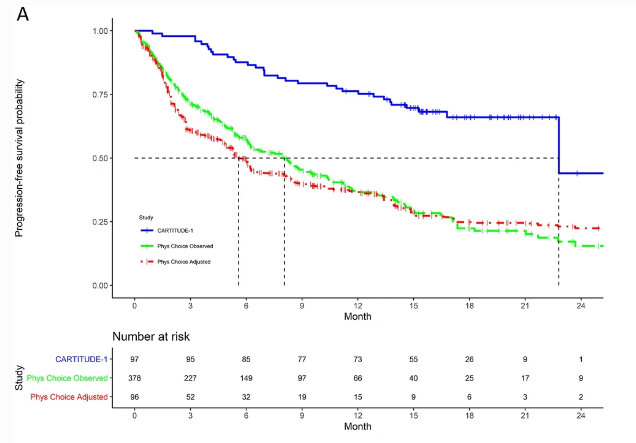
对接受cilta-cel和医生选择的治疗的患者的总生存期和无进展生存期的Kaplan-Meier估计
进行meta分析来比较cilta-cel和医生选择的治疗在难治性和复发性多发性骨髓瘤中的有效性。
接受 cilta-cel治疗的患者的数据来自CARTITUDE-1临床试验。接受医生选择的治疗的患者数据来自 Flatiron数据库、LocoMMotion研究、达雷妥尤单抗临床试验(POLLUX、EQUULEUS和CASTOR)、OncologyInformationService (OIs) 和MAMMOTH研究。
结果表明,与医生选择的治疗相比,cilta-cel显着提高了总生存期、总缓解率和无进展生存期[10]。接受Cilta-cel治疗的患者获得总体反应的可能性是接受医生选择的治疗的患者的86 倍。
cilta-cel的疗效还与难治性或复发性多发性骨髓瘤患者的现实世界标准治疗(RW SOC)进行了比较[11]。来自 Flatiron数据库的RW SOC 患者组接受了埃罗妥珠单抗、泊马度胺、达雷妥尤单抗、卡非佐米 和 伊沙佐米。该组患者的总生存期和无进展生存期低于CARTITUDE-1临床试验的患者。
小结
复发和难治性多发性骨髓瘤的治疗负担很高。较新的治疗方法如塞利尼索、belantamab mafodotin 和idecabtagene Vicleucel 无法产生令人满意的结果。与医生选择的治疗方法相比,Cilta-cel显着提高了复发性和难治性多发性骨髓瘤患者的总生存期和无进展生存期。
这项CARTITUDE-4试验的结果表明,与标准治疗方案相比,单次输注cilta-cel可以显着提高对来那度胺无反应的多发性骨髓瘤患者的生存率。
这种突破性药物有望挽救所有难治性和复发性多发性骨髓瘤患者的生命。


