读书报告 | NeoTrio研究: 帕博利珠联合达拉菲尼和曲美替尼新辅助治疗BRAF突变黑色素瘤的II期研究
时间:2025-02-20 12:08:45 热度:37.1℃ 作者:网络
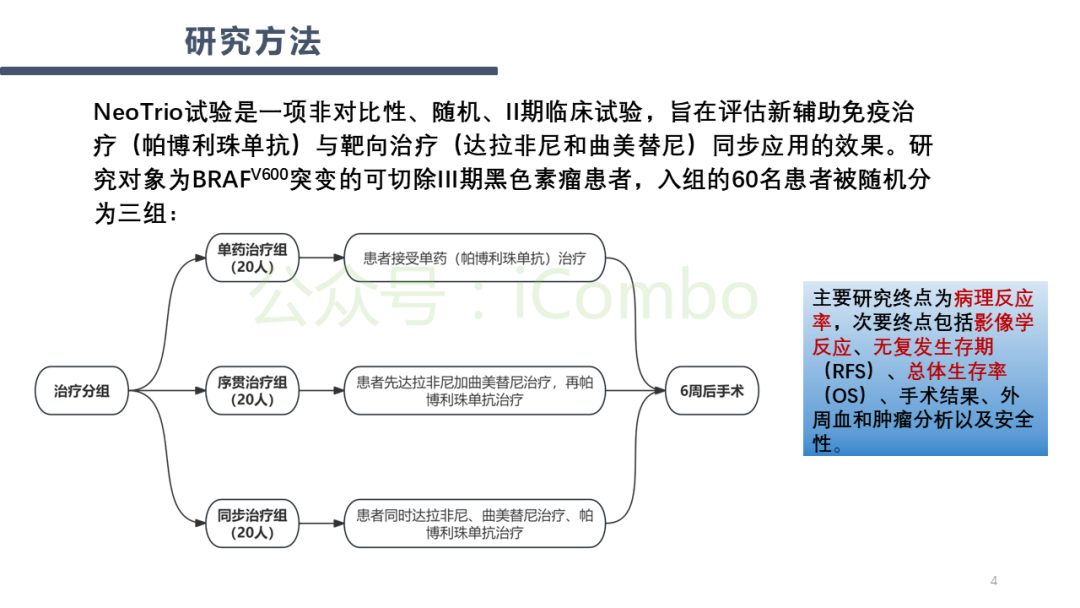
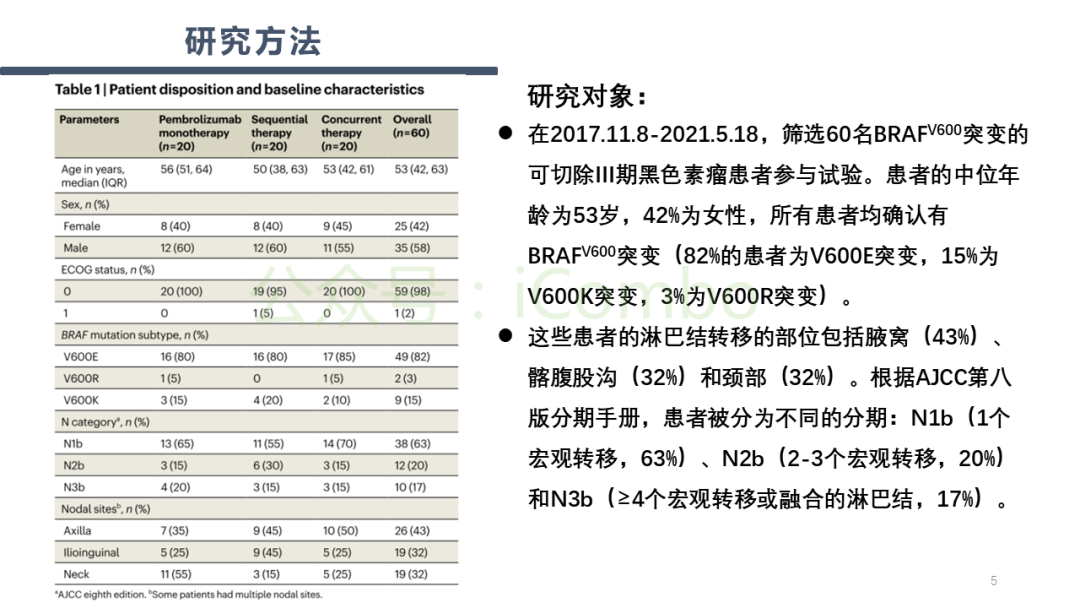
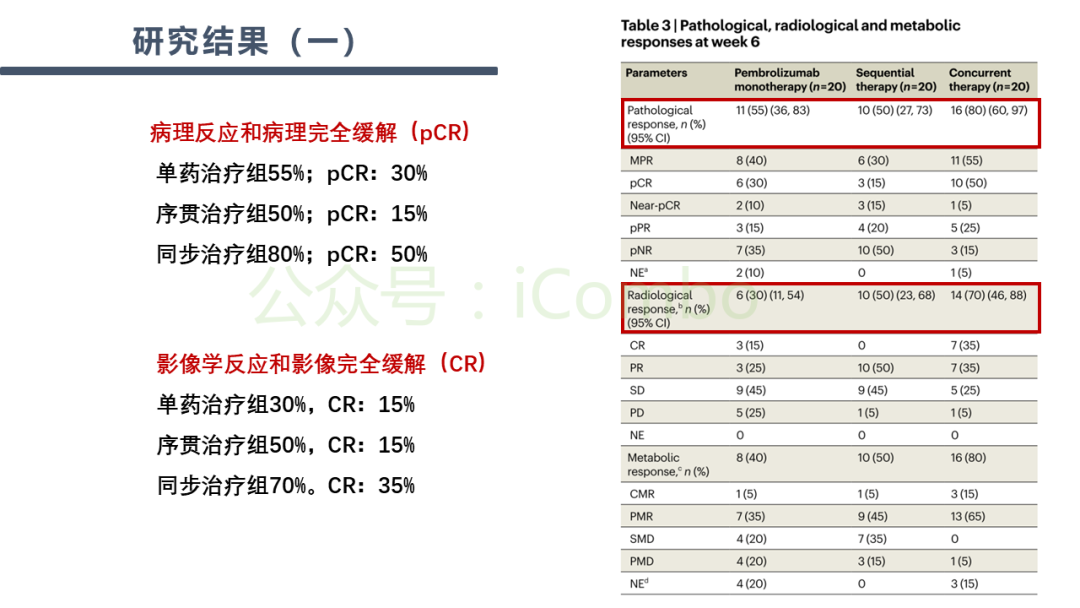
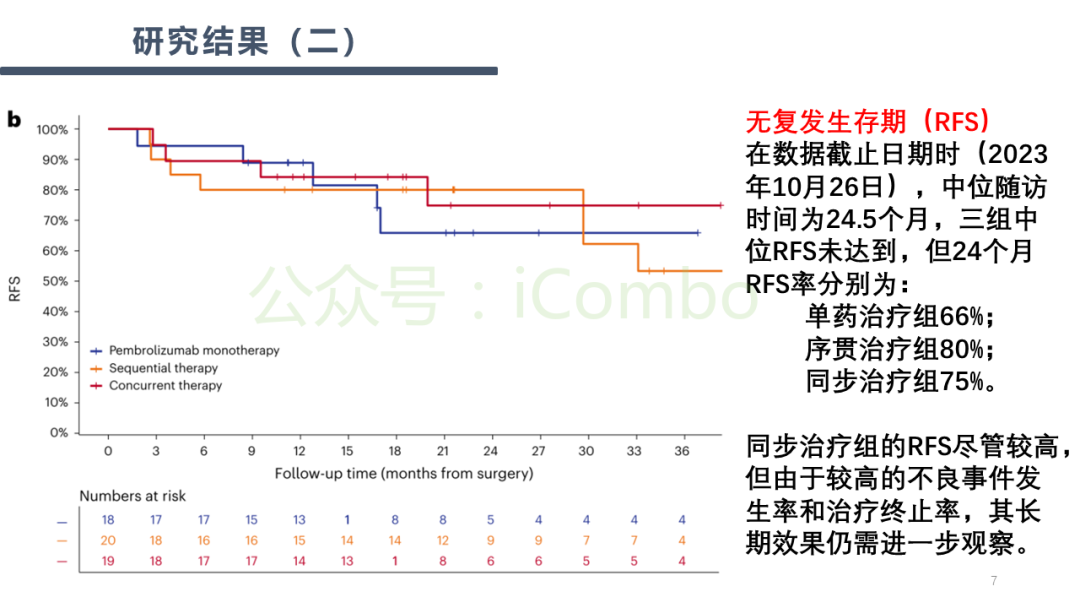
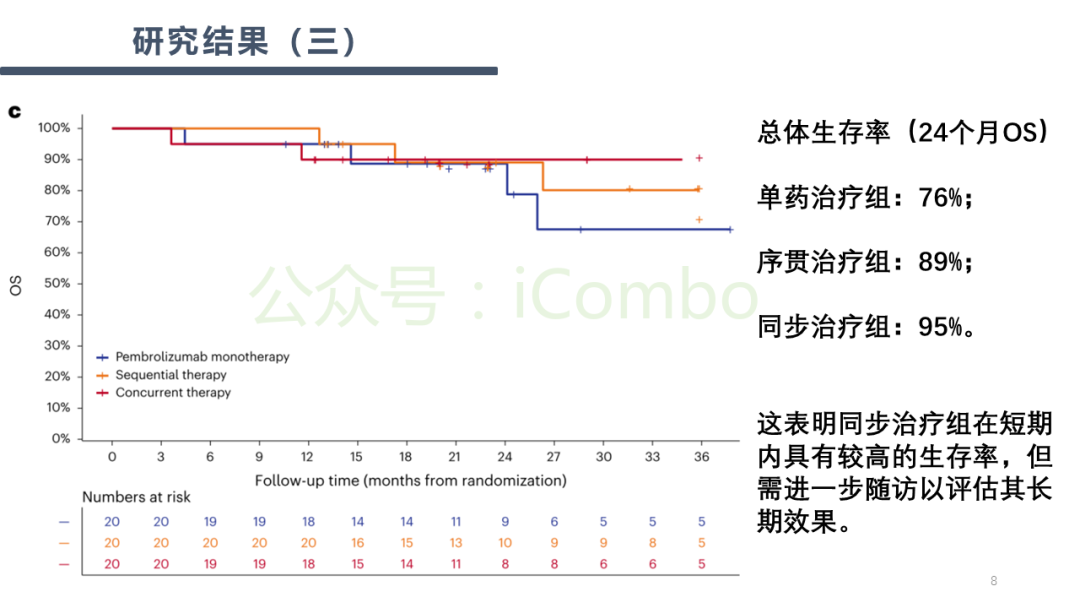
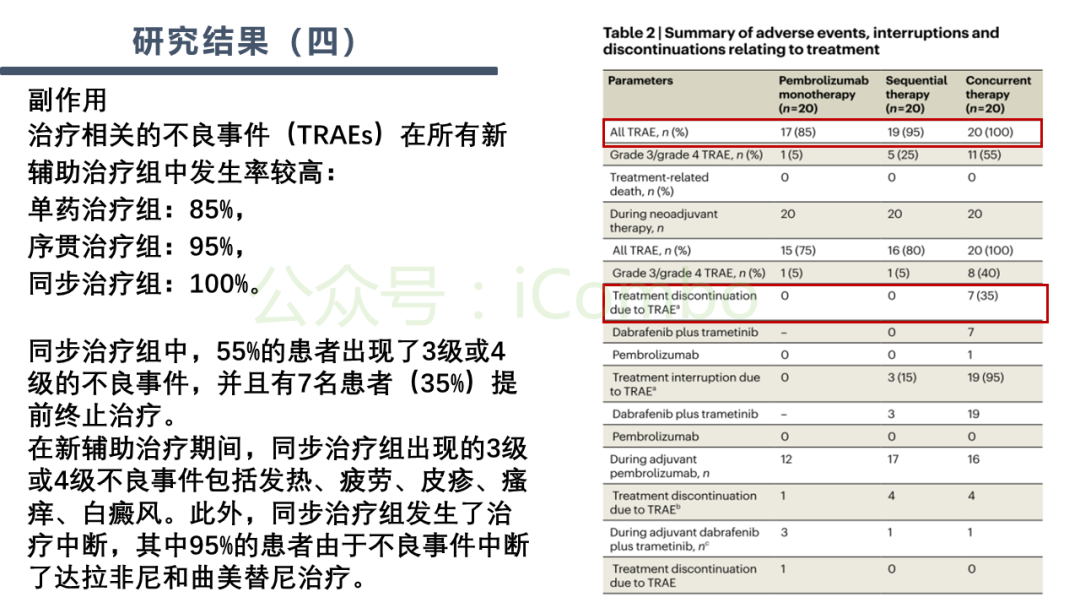
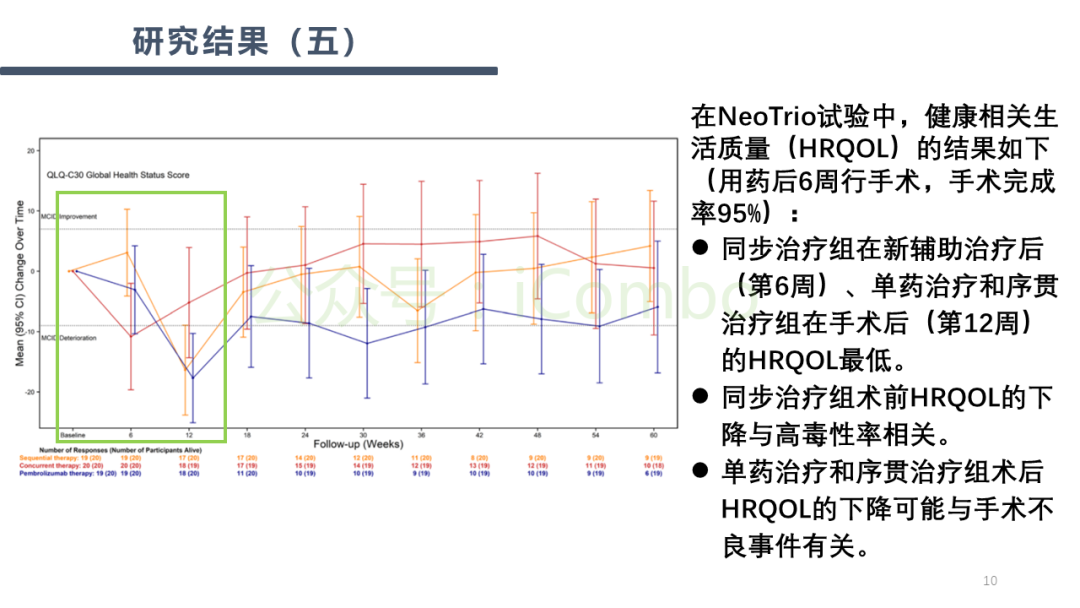
导读 BRAF和MEK抑制剂能够提升BRAFV600突变患者的整体反应率(ORR),而免疫检查点抑制剂则通常能带来更持久的治疗应答。理论上,将免疫检查点抑制剂与BRAF和MEK抑制剂相结合,可能会实现更佳且更持久的治疗效果。先前的临床前模型和患者活检样本分析证据显示,抑制BRAFV600驱动的癌基因有利于激发抗肿瘤免疫反应。 在KEYNOTE-022研究的第一阶段中共有15名患者接受了抗PD-1抗体pembrolizumab联合BRAF抑制剂dabrafenib(D)和MEK抑制剂trametinib(T)的治疗方案。在另一项第一阶段试验中,8名和39名患者分别接受了D+T联合抗PD-L1抗体atezolizumab的治疗。这两项研究所得出的疗效数据呈现出一致性:BRAF、MEK和免疫检查点抑制剂的联合治疗方案分别产生了73%和72%的ORR;中位无进展生存期(PFS)分别为15.4个月和12.9个月。值得注意的是,肿瘤活检样本分析表明,在pembro+D+T联合治疗后,观察到CD8+ T细胞的肿瘤浸润增加,以及PD-L1和T细胞炎症基因表达的上升。 KEYNOTE-022的随机、双盲、2期研究对pembro+D+T三联组合疗法与D+T双联组合疗法加安慰剂的疗效进行了比较。在中位随访9.6个月时,尽管PFS的主要终点在三联组与双联组之间并未显示出统计学意义上的显著差异,但三联组的数值更高(16.0个月对比10.3个月;风险比HR为0.66;p=0.043)。而在平均中位随访时间延长至36.6个月后,研究结果显示,三联组在持续反应时间(DOR,25.1个月对比12.1个月)、PFS(16.9个月对比10.7个月)和总生存期(OS,未达到对比16.3个月)上均有显著改善。 研究方法:NeoTrio试验是一项非比较、随机、二期临床试验,共纳入60名患者,随机分配到三组:单独使用pembrolizumab(n=20)、序贯治疗(dabrafenib加trametinib后跟pembrolizumab;n=20)或同时治疗(三联治疗;n=20)。治疗后进行手术和辅助治疗。主要终点是病理反应,次要终点包括影像学反应、无复发生存、总生存、手术结果、外周血和肿瘤分析以及安全性。 实验结果:病理反应率:pembrolizumab组为55%(11/20,包括6个病理完全反应pCR),序贯治疗组为50%(10/20,3个pCR),同时治疗组为80%(16/20,10个pCR),均达到主要终点。治疗相关不良事件:在新辅助治疗期间,75-100%的患者受到影响,同时治疗组有7例早期停药。2年无事件生存率:pembrolizumab组为60%,序贯治疗组为80%,同时治疗组为71%。复发情况:主要病理反应后的复发在靶向治疗组更为常见,表明加入靶向治疗可能降低了反应的“质量”。 关键结论:尽管联合治疗组的病理反应率最高,但考虑到毒性增加和可能失去免疫治疗的治愈潜力,研究者不建议在黑色素瘤的新辅助治疗中联合使用免疫治疗和靶向治疗。研究还发现,病理反应是无复发生存的更好预测指标,比影像学反应措施更准确。 讨论:研究结果表明,尽管联合治疗在短期内显示出较高的病理反应率,但长期随访对于确定反应的持久性和质量至关重要。此外,研究还探讨了新辅助治疗对患者生活质量的影响,发现联合治疗组在手术前生活质量下降最为明显,而pembrolizumab单药治疗组在手术后生活质量下降最为显著。 研究限制:NeoTrio试验的样本量较小,限制了对长期生存和生活质量趋势的清晰解读。此外,试验设计并未对三组间进行统计学比较,这限制了对结果的解释。 未来方向:未来的研究应关注新的免疫治疗方法,以针对对免疫治疗无反应的患者提供持久反应。同时,需要进一步研究病理反应与代谢反应之间的关系,以及如何通过生物标志物驱动的治疗研究来优化治疗策略(Nat Med. 2024 Sep;30(9):2540-2548. doi: 10.1038/s41591-024-03077-5)。