电子科技大学肖波团队《Adv Sci》:纳米工程菌通过增强光免疫疗法和微生物色氨酸代谢口服治疗结直肠癌
时间:2025-02-08 12:08:56 热度:37.1℃ 作者:网络
结直肠癌(CRC)是全球主要的健康威胁之一。尽管手术、化疗和放疗等传统治疗方法取得了进展,但CRC的发病率和死亡率仍在持续上升。免疫治疗因其能够引起持久和可持续的抗肿瘤反应而备受关注,但困扰临床免疫治疗CRC的两大难题仍然没有解决:一是CRC存在特定的免疫抑制性肿瘤微环境。这种微环境不仅能够抑制抗肿瘤免疫反应,还为肿瘤细胞提供了逃逸免疫监视条件。二是肠道菌群失调。肠道内的微生物不仅参与肠道的局部免疫反应,还通过血液-肠道屏障与全身免疫系统相互作用,而肠道菌群失调,则可能通过改变免疫细胞的功能或数量,削弱免疫治疗的效果。因此,从改善肿瘤免疫抑制微环境和缓解肠道菌群失调方面进行药物开发,具有重要意义。
鉴于此,电子科技大学附属医院•四川省人民医院、电子科技大学医学院肖波教授团队开发了一种新型纳米细菌平台LR-S-CD/CpG@LNP,通过整合光疗法、免疫治疗和微生物代谢调节三重作用机制,不仅能够通过原位疫苗效应有效抑制原发性结直肠肿瘤的生长,还能调节肠道菌群预防和治疗CRC的肝转移。相关工作以“Nano-Armed Limosilactobacillus reuteri for Enhanced Photo-Immunotherapy and Microbiota Tryptophan Metabolism against Colorectal Cancer”为题在线发表在《Advanced Science》。论文通讯作者为电子科技大学肖波教授、俎梦航博士和西南大学石潇潇副教授。
【文章要点】
本研究开发了一种响应活性氧(ROS)的细菌基纳米平台LR-S-CD/CpG@LNP。该系统将免疫佐剂(CpG)和以桑叶为碳源的碳点(CD)共载的桑叶脂质纳米粒子(CD/CpG@LNPs)通过ROS响应性连接物连接到有益菌Limosilactobacillus reuteri(LR)表面。通过一系列实验,包括光学性能、理化性质分析、ROS响应性释放、细菌活力测试和胃肠道稳定性评估,证实了该有益菌药递送平台的成功构建(图1)。

图1 LR-S-CD/CpG@LNPs的制备及其理化性质表征
体外实验表明,在近红外光(NIR)照射下,CD/CpG@LNPs的光热和光动力特性诱导了原位结直肠肿瘤细胞发生免疫原性死亡(ICD),将"冷"肿瘤转变为"热"肿瘤(图2A-J)。产生的新抗原和释放的CpG作为有效的原位疫苗刺激树突状细胞(DC)的成熟,继而激活抗肿瘤抗原特异性免疫反应(图2K)。

图2 CD/CpG@LNPs的体外促凋亡、免疫原性死亡和DC成熟作用
体内生物分布实验表明,与单独使用CD/CpG@LNPs相比,口服基于益生菌LR的LR-S-CD/CpG@LNPs显著延长纳米药物在结肠中的停留时间,即延长至72 h(图3A,B)。此外,本研究采用的ROS响应型连接子,增强了CD/CpG@LNPs在结直肠肿瘤中的释放、穿透及积累能力(图3C-D)。

图3口服CD/CpG@LNPs或LR-S-CD/CpG@LNPs联用NIR的肿瘤积累和体内分布
体内治疗实验表明,与CD/CpG@LNPs相比,LR表面结合的CD/CpG@LNPs表现出显著增强的抗肿瘤效果。特别是在NIR照射下,LR-S-CD/CpG@LNPs组的肿瘤抑制效果更为显著,肿瘤数量减少了1.9倍,且肿瘤体积大幅减小(图4A-E)。LR不仅通过其本身的生物学特性帮助纳米颗粒在结肠中更长时间停留,提高了药物在肿瘤微环境中的积累,还通过增强系统性抗肿瘤免疫反应,进一步增强了CD/CpG@LNPs的治疗效力(图4F-I)。
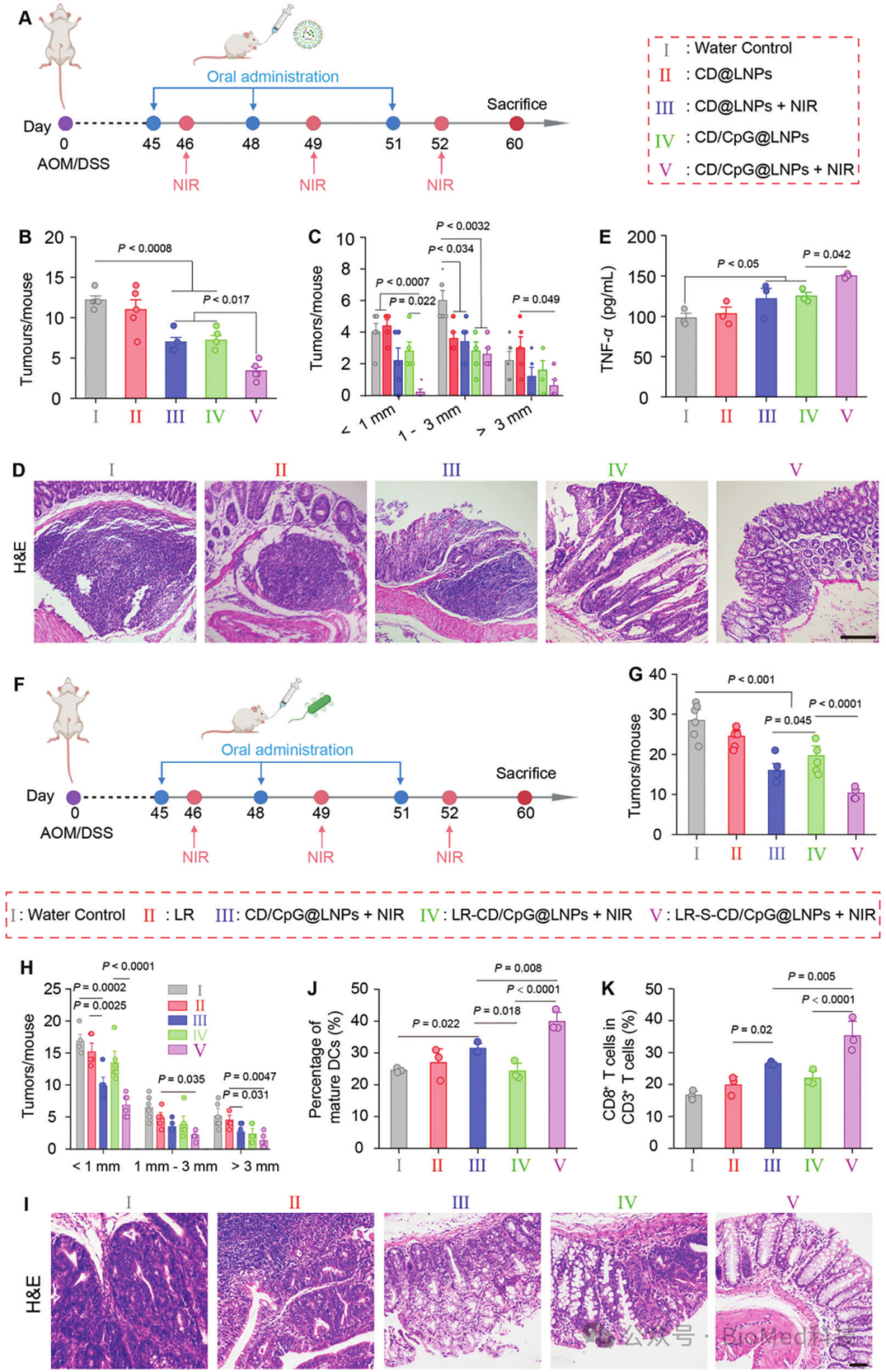
图4口服CD/CpG@LNPs或LR-S-CD/CpG@LNPs联用NIR对原位CRC的治疗效果
进一步的体内药效实验结果表明,LR-S-CD/CpG@LNPs的光免疫治疗和肠道微生物代谢物调节共同抑制了原位结直肠肿瘤和肝转移(图5A-F)。进一步的研究机制发现该治疗方案显著增加了有益菌群(如Lactobacillus和Alistipes)的丰度,同时降低了有害菌群(如Enterobaçteriaceae)的比例(图5G-I)。同时,代谢组学分析表明,LR-S-CD/CpG@LNPs处理组中Lactobacillus丰度的上调导致吲哚-3-醛(I3A)水平升高,这是一种通过芳香烃受体发挥作用的色氨酸代谢物,可以刺激CD8+ T细胞产生干扰素-γ(IFN-γ),从而增强抗肿瘤免疫应答(图5J-M)。
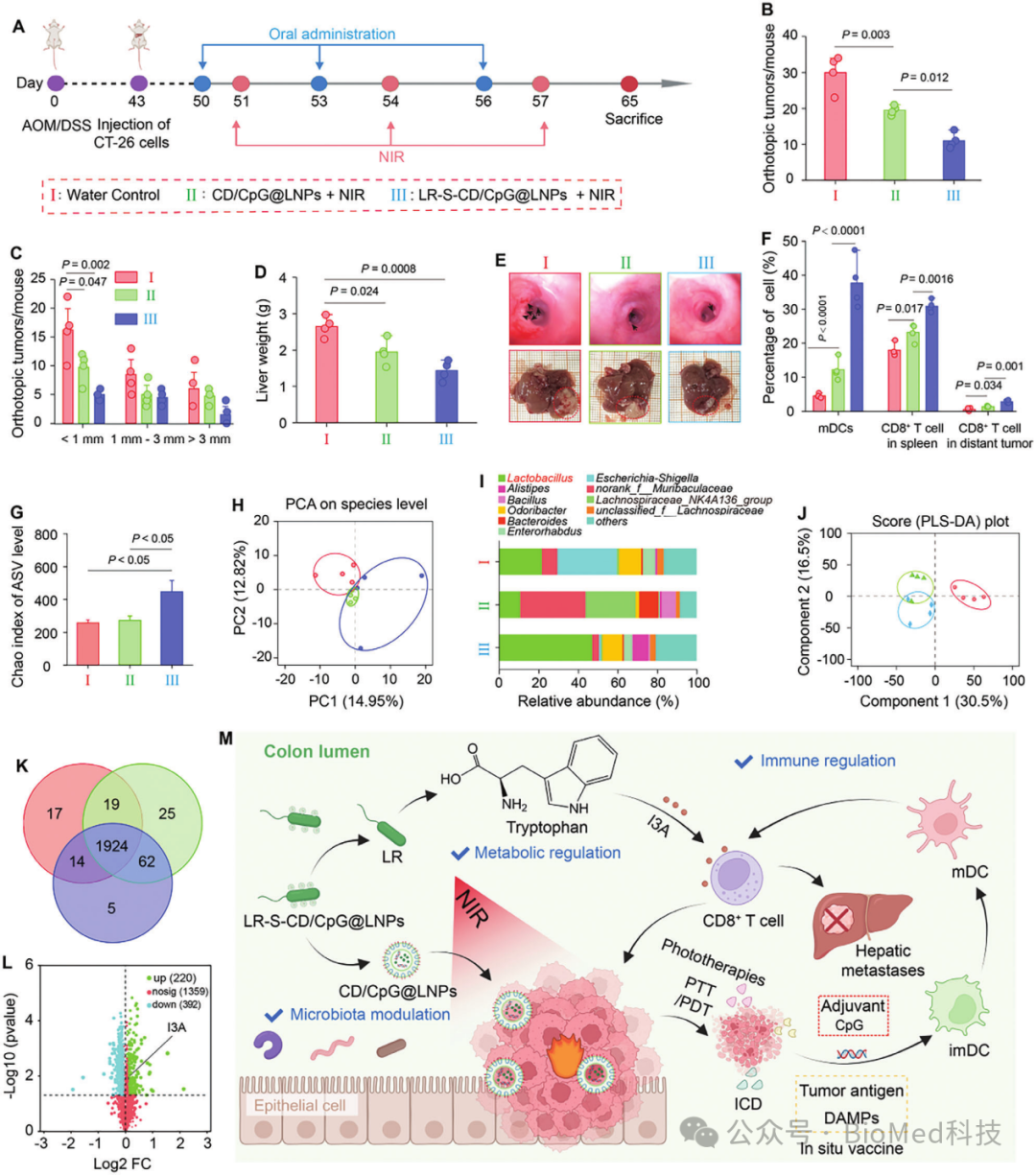
图5口服LR-S-CD/CpG@LNPs联用NIR对原位CRC和肝转移的体内治疗作用、肠道微生物群和代谢调节
【结论与展望】
综上所述,本研究基于光治疗诱导的原位疫苗与益生菌结合,开发了LR-S-CD/CpG@LNPs这一创新性治疗系统,用于CRC及其转移的高效光/免疫治疗及微生物代谢调控。研究中采用ROS可裂解连接子,将LR与包裹CD和CpG的桑叶脂质纳米颗粒(CD/CpG@LNPs)相连接,实现了肠腔滞留药物在肿瘤区域的精准释放。通过NIR照射,肿瘤区域的温度升高和细胞毒性ROS水平显著提升,诱导肿瘤ICD的同时形成原位疫苗,促进了DCs的成熟以及后续的抗肿瘤特异性免疫反应。此外,LR代谢色氨酸生成I3A进一步增强抗肿瘤免疫反应,并调控肠道微生物群,增加有益菌(如Lactobacillus和Alistipes)的丰度,降低有害菌(如Enterobaçteriaceae)的丰度。本研究验证了该基于有益菌的抗肿瘤原位疫苗系统(LR-S-CD/CpG@LNPs)在CRC及其肝转移治疗中的显著疗效,为未来CRC治疗提供了全新的方法与思路(图6)。

图6 口服LR-S-CD/CpG@LNPs联用NIR实现肿瘤积聚、原位疫苗和激活针对CRC的全身抗肿瘤免疫反应示意图
作者信息
肖波:电子科技大学附属医院•四川省人民医院、电子科技大学医学院教授,博士生导师。主要从事慢性炎症性疾病和恶性肿瘤治疗相关纳米药物系统研究。先后入选国家级青年人才(生物与新医药技术)、“全球前2%顶尖科学家”(药学/生物医学工程领域)和重庆市杰出青年基金获得者(医学领域)等。近年来,以独立或最后通讯作者身份在Gastroenterology、Advanced Materials、ACS Nano、Advanced Drug Delivery Reviews、Journal of Controlled Release、Acta Pharmaceutica Sinica B、Advanced Science和Advanced Functional Materials等国际权威期刊上发表学术论文80余篇,申请美国专利3项(授权1项)和中国专利10余项(授权4项,转让1项)。担任Research、Acta Pharmaceutica Sinica B和Asian J. Pharm. Sci.等期刊青年编委、中国药学会智能药物专委会委员和中国生物材料学会医疗器械与生物材料分会委员等。
石潇潇:副教授,2022年6月毕业于厦门大学,2022年7月就职于西南大学。主要研究方向是微/纳米药物递送系统用于疾病的诊疗一体化研究。目前参与发表SCI论文20余篇,其中以第一作者、通讯作者(含共同)身份在Acc. Mater. Res.、Nano Today、Adv. Funct. Mater.、Adv. Sci.、Biomaterials、Small Methods等高水平学术期刊发表论文10余篇,影响因子大于10的论文8篇。此外,申请人已取得国家发明专利7项(授权),主持国家自然科学基金、重庆市自然科学基金面上项目、西南大学中央高校基本业务费各一项。
原文链接:
https://advanced.onlinelibrary.wiley.com/doi/full/10.1002/advs.202410011


