【病例报告】HTRA丝氨酸肽酶1基因杂合突变致相关脑小血管病一家系报道
时间:2024-11-23 16:01:36 热度:37.1℃ 作者:网络
摘要:HTRA丝氨酸肽酶1(HTRA1)相关脑小血管病(CSVD)较罕见,尽早诊断和治疗可改善预后。作者报道南昌大学第二附属医院神经内科收治的1例37岁、男性患者,以一过性右侧肢体无力为首发症状,影像学提示脑白质病变,基因检测显示HTRA1(c.854C> T/p.Pro285Leu)杂合突变,最终诊断为HTRA1相关CSVD。对其家系成员进行调查,其特点为:罹患缺血性脑血管病,伴颈椎、腰椎间盘突出,男性患者伴脱发,部分患者存在认知功能障碍,男性比女性发病年龄早,发病年龄逐代提前。因此,对于青年缺血性脑血管病伴随脱发、认知功能障碍、颈椎或腰椎间盘突出,影像学提示明显脑白质病变,尤其不伴有常见脑血管病危险因素的患者,应追问家族史,并进行基因检测筛查HTRA1基因突变位点。
HTRA丝氨酸肽酶1(high-temperature requirement A serine peptidase 1, HTRA1)基因纯合或复合杂合突变可导致伴有皮质下梗死和白质脑病的常染色体隐性遗传性脑动脉病(cerebral autosomal recessive arteriopathy with subcortical infarcts and leukoencephalopathy, CARASIL),HTRA1基因杂合突变可致常染色体显性遗传性脑小血管病(cerebral small vessel disease,CSVD),在线人类孟德尔遗传数据库(OMIM616779, https:∥omim.org)中将HTRA1基因杂合突变导致的伴有皮质下梗死和白质脑病的常染色体显性遗传性脑动脉病(cerebral autosomal dominant arteriopathy with subcortical infarcts and leukoencephalopathy,CADASIL)称为CADASIL2型,也可将其称为HTRA1相关常染色体显性遗传病。HTRA1基因杂合突变为常染色体显性遗传性CSVD的第二大病因,该显性遗传性CSVD的典型影像学特点包括白质高信号(white matter hyperintensity, WMH)、腔隙、扩大的血管周围间隙(enlarged perivascular spaces, EPVS)以及微出血灶。HTRA1相关CSVD的临床症状包括神经系统症状和神经系统外症状,神经系统症状主要特征为反复卒中发作和认知功能下降,易被漏诊。HTRA1相关CSVD占遗传性CSVD的5%。目前,针对HTRA1相关CSVD的大型研究报道较少,其基因型与表型的相关性尚未清楚。现收集并分析1例我院神经内科收治的HTRA1相关CSVD患者的病历资料及其家系成员相关特点,以提高临床医师对该病的认识。
患者
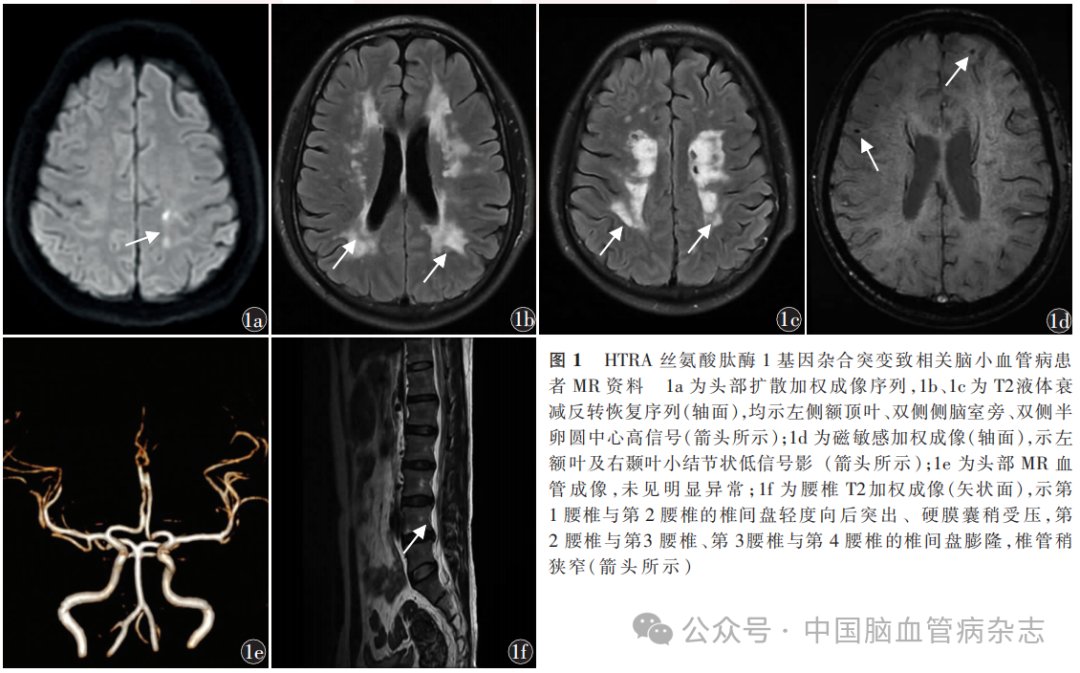
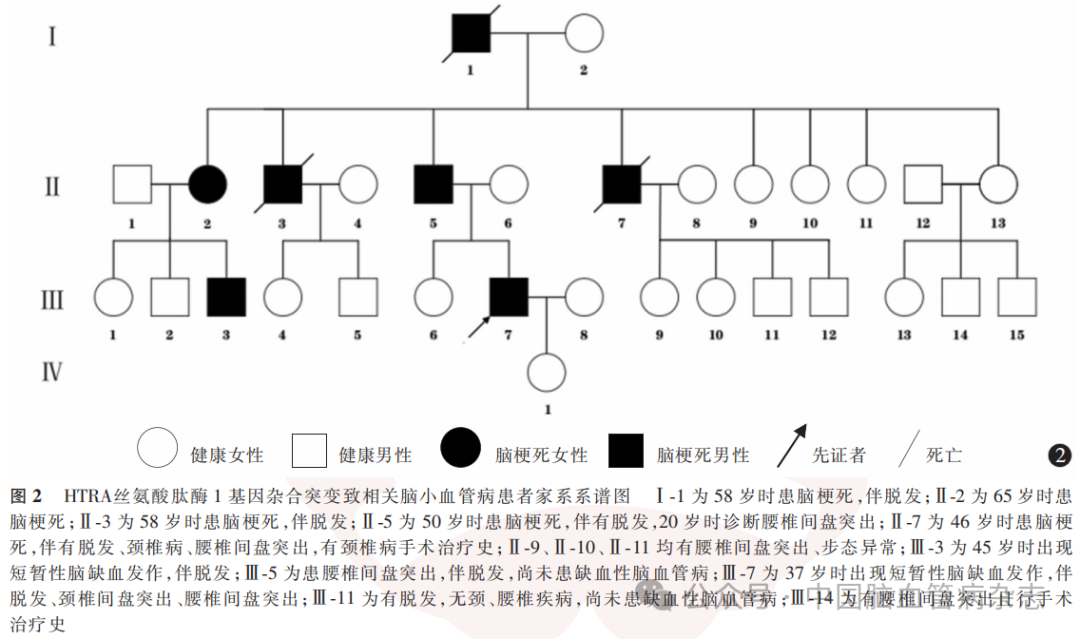
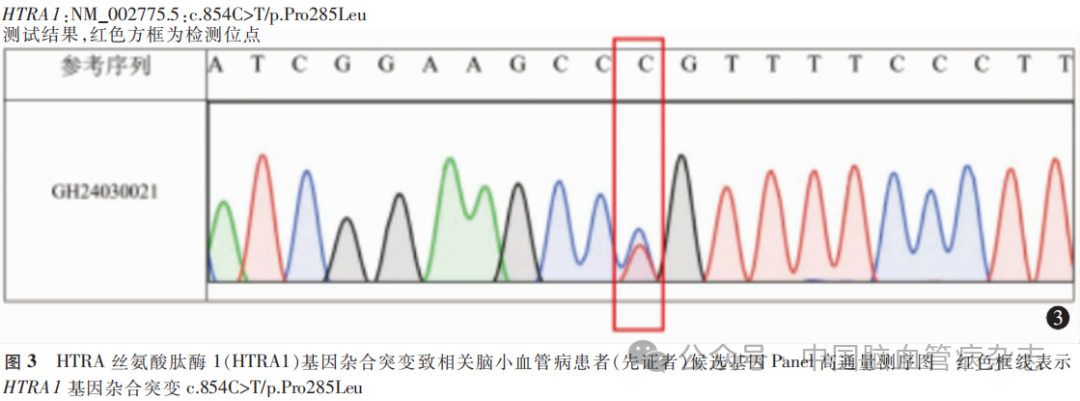
男,37岁,因“一过性右侧肢体无力3d”于2024年3月5日收入南昌大学第二附属医院神经内科。入院前3d,患者无明显诱因突发右侧肢体无力,以右下肢行走不稳为著,持续约1 min症状自行缓解,无言语不清、口角歪斜、视物模糊等。为查明原因,患者于2024年3月5日就诊于我院神经内科门诊,以“脑梗死”收入神经内科。既往腰椎间盘突出病史18年、额部脱发史8年、颈椎间盘突出史4年,无高血压病、糖尿病、冠心病史;2004年行阑尾切除术。入院时体温36.6℃,脉搏105/min,呼吸20次/min,血压147/99mmHg。额部脱发。心、肺、腹体格检查未见异常。神经系统体格检查:意识清楚,言语流利,理解力、定向力、注意力、计算力均正常。脑神经体格检查正常。双侧肢体痛触觉正常,四肢肌力、肌张力正常。双侧指鼻试验、跟膝胫试验稳准,龙贝格征阴性。四肢腱反射正常,双侧病理征未引出,脑膜刺激征阴性。初步诊断“脑梗死”。入院后完善相关检查:血脂、C反应蛋白、B型脑钠肽、糖化血红蛋白、餐后2 h血清葡萄糖测定、抗核抗体谱、血清抗中性粒细胞胞质抗体谱等实验室检查均未见异常。常规心电图、动态心电图、胸部CT、超声心动图、发泡试验均正常。24 h动态血压监测显示,平均收缩压128mmHg(正常参考值:<130 mmHg),平均舒张压80mmHg(正常参考值:<80mmHg);日间平均收缩压、平均舒张压分别为126、80mmHg,夜间平均收缩压、平均舒张压分别为131、79mmHg。蒙特利尔认知评估量表评分21分(总分30分,评分≥26分为正常),轻度认知功能障碍(理解力、定向力、注意力、计算力基本正常,执行力、记忆力减退),自理能力正常。头部MR扩散加权成像序列(图1a)、T2液体衰减反转恢复序列(图1b,1c)示左侧额顶叶、双侧侧脑室旁、双侧半卵圆中心高信号,提示左侧额顶叶急性-亚急性期脑梗死,脑白质疏松,脑内多发缺血灶及陈旧性脑梗死;磁敏感加权成像示左额叶及右颞叶小结节状低信号影,提示微出血灶(图1d)。MR血管成像未见明显异常(图1e)。腰椎MRT2加权成像示第1腰椎与第2腰椎的椎间盘轻度向后突出,硬膜囊稍受压,第2腰椎与第3腰椎、第3腰椎与第4腰椎的椎间盘膨隆,椎管稍狭窄(图1f)。经颅多普勒超声未见明显异常。结合病例特点:37岁、一过性右侧肢体无力,无明显卒中危险因素,伴脱发、腰椎间盘突出,影像学提示脑白质病变,考虑存在遗传性CSVD的可能。追问病史,患者的祖父(Ⅰ-1)、大姑(Ⅱ-2)、大伯(Ⅱ-3)、父亲(Ⅱ-5)、叔父(Ⅱ-7)均有脑梗死病史,分别于58、65、58、50、46岁发病;其祖父(Ⅰ-1)、大伯(Ⅱ-3)、父亲(Ⅱ-5)、叔父(Ⅱ-7)均有脱发;其父亲(Ⅱ-5)、叔父(Ⅱ-7)、3位姑姑(Ⅱ-9、Ⅱ-10、Ⅱ-11)均有腰椎间盘突出病史或伴步态异常;其一位表兄(Ⅲ-3)曾有短暂性脑缺血发作史且伴脱发,三位表兄(Ⅲ-5、Ⅲ-11、Ⅲ-14)虽未患缺血性脑血管病,但存在脱发或腰椎间盘突出(图2)。进一步对患者及其家系成员进行全外显子组行遗传病候选基因Panel高通量测序,结果显示,先证者HTRA1基因发现1个杂合突变,即c.854C> T/p.Pro285Leu(图3),其父亲的基因检测同样为c.854C>T/p. Pro285Leu,家系中其他成员由于各种原因未行基因检测。故诊断为HTRA1基因杂合突变致HTRA1相关CSVD。给予抗血小板聚集、改善循环、控制血压等综合治疗。共治疗7d,患者右侧肢体无力未再发作,好转出院。出院后继续行抗血小板聚集、改善循环等对症治疗。已电话随访7个月,患者未再发生上述症状。
讨论
CSVD是一种与年龄相关的散发性疾病,少数患者被确定为家族性单基因病因,约占5%,其中常见的类型有NOTCH 3基因突变导致的CADASIL、HTRA1基因纯合突变或复合杂合突变导致的CARASIL、HTRA1基因杂合突变导致的HTRA1相关常染色体显性遗传病、COL4A1/2基因突变导致的Ⅳ型胶原蛋白A1/2脑小动脉病以及罕见的遗传性毛细血管扩张症伴海绵状血管瘤、FOXC1和PITX2基因相关的CSVD等。
研究报道,CADASIL分为CADASIL1型和CADASIL 2型,前者由NOTCH3基因突变引起,是最常见的遗传性CSVD,而HTRA1相关常染色体显性遗传性CSVD被称为CADASIL 2型。与CARASIL不同,杂合子HTRA1基因突变相关CSVD由HTRA1的双等位基因突变引起。本例患者基因测序结果显示HTRA1基因1个杂合突变(c.854C> T/p.Pro285Leu),已有研究报道该突变位点,结合患者临床表现及影像学特征,符合CADASIL 2型特点。该突变位点(NM_002775.5:c.854C> T)以杂合形式在至少4例CSVD相关患者中被检出,其共同特征为卒中、脱发、腰椎间盘突出、认知功能下降、步态障碍,影像学上显示脑白质病变、腔隙性脑梗死和脑微出血。
HTRA1属于高度保守的丝氨酸蛋白酶家族,参与了多项生理功能,其功能丧失可致脱发、骨形成异常、椎间盘变性、毛细血管扩张伴出血和血管纤维化等,可解释本例患者有脱发及腰椎间盘突出的原因。HTRA1蛋白由Kazal丝氨酸蛋白酶抑制剂结构域、胰蛋白酶样丝氨酸蛋白酶结构域等5个结构域共同构成,其中胰蛋白酶样丝氨酸蛋白酶结构域受影响最大,其次是Kazal丝氨酸蛋白酶抑制剂结构域,且位于胰蛋白酶样丝氨酸蛋白酶结构域中的第250~300位氨基酸及其附近的氨基酸最常受到影响。本例患者及其父亲HTRA1基因c.854T>C杂合突变,该突变可导致第285位脯氨酸变成亮氨酸,符合文献报道中的胰蛋白酶样丝氨酸蛋白酶结构域。
HTRA1相关常染色体显性遗传病的神经系统症状包括反复的神经功能受损症状(腔隙性脑梗死、短暂性脑缺血发作、脑出血相关症状)、步态异常、认知功能障碍、情绪改变以及球麻痹等,其神经系统外表现包括腰部疼痛、腰椎间盘突出、颈椎间盘突出及脱发等。此外,还可出现精神障碍、色盲、自主神经小纤维神经病变、脑积水和多发性蛛网膜囊肿等。头部影像学表现包括T2加权成像显示融合的皮质下WMH、腔隙性脑梗死、脑微出血、少数胼胝体受累、通常不累及U型纤维等。本例患者具有一过性右侧肢体无力、脱发、腰椎间盘突出、认知功能下降的临床特点以及脑白质病变等影像学特征,均与文献报道相符合。
HTRA1相关CSVD患者脑小血管的病理组织学特点包括血管内膜增厚、外膜纤维化、平滑肌细胞变性和丢失以及小血管内弹性层分层、分裂现象,其发生机制与炎症介质引起内皮细胞损伤而致内质网应激有关。目前,电子显微镜下尚未发现HTRA1相关CSVD患者的平滑肌细胞表面有嗜锇颗粒沉积,有研究表明皮肤活组织检查结果可与典型CADASIL的鉴别提供依据。本例患者未行皮肤活组织检查。
在药物二级预防方面,小动脉病变一直缺乏有效的治疗药物,尤其是遗传性脑小动脉病,相关循证医学研究报道较少。有研究结果表明,阿司匹林、西洛他唑、双嘧达莫对CSVD疗效的差异无统计学意义(P>0.05),双联与单一抗血小板聚集药物治疗效果的差异无统计学意义(P>0.05),但双联用药可增加出血的风险,单硝酸异山梨酯和西洛他唑联合用药可能会改善血液循环及认知功能。
HTRA1相关CSVD的临床和影像学表现均与CARASIL相似,与CARASIL相比,HTRA1相关CSVD发生卒中或头痛的差异无统计学意义(P>0.05),但HTRA1相关CSVD男性多发,男性患者HTRA1基因杂合突变风险约为女性患者的2倍,但临床症状较轻,进展较慢,卒中发病年龄较晚,认知功能障碍较轻,步态障碍发生比例较低,无典型的CARASIL神经系统外表现,且脱发和脊柱疾病等发生率较低,大部分CARASIL患者的父母为近亲婚姻。HTRA1相关CSVD(也称CADASIL2型)与CADASIL1型患者的年龄、性别、血管危险因素、神经功能症状、脱发的差异均无统计学意义(P>0.05),但杂合子HTRA1相关CSVD患者的脊柱疾病比例更高,累及前颞叶的WMH比例更低。本例患者为青年男性,有一过性右侧肢体无力症状,无明显脑血管病危险因素,无偏头痛,伴随脱发、认知功能障碍、腰椎间盘突出,WMH位于额顶叶及侧脑室旁,最终经基因检测证实为HTRA1相关CSVD。本例先证者家系中患者特点为有卒中病史,合并颈椎疾病、腰椎间盘突出,男性患者伴脱发,部分患者存在认知功能障碍,男性比女性发病年龄早,发病年龄逐代提前。
对于青年缺血性脑血管病伴脱发、认知功能障碍、颈椎病或腰椎间盘突出,且影像学提示明显脑白质病变,尤其不伴有常见的脑血管病危险因素者,应追问家族史,并进行基因检测筛查HTRA1基因突变位点。本研究缺陷:该家系中除患者(先证者)及其父亲进行了基因检测,其余有相关表现的患者因去世或经济等原因未行基因检测,故家系资料欠完整。


