BMT:CD19 CAR-T治疗NHL伴风湿性自身免疫性疾病:一项倾向性评分匹配研究
时间:2023-09-02 14:00:16 热度:37.1℃ 作者:网络
近年来CD19 CAR-T细胞治疗的适应症和可用性大大提高,且已应用于B细胞恶性肿瘤之外的疾病,特别是在自身免疫性疾病中,B细胞消耗也可能是有益的。最近的一项研究表明,CD19 CAR-T细胞可以诱导难治性系统性红斑狼疮(SLE)患者持久缓解。
然而使用CD19 CAR-T细胞疗法治疗B细胞恶性肿瘤并发风湿性自身免疫性疾病的患者具有独特挑战。风湿性自身免疫性疾病中的B细胞功能失调,活化的T细胞由于对凋亡的抵抗而表现出延长的存活,同时表现出细胞毒性降低和持续抗原刺激的衰竭表型。此外,输注自身反应性T细胞可能会恶化潜在的自身免疫性疾病。此外,患者经常接受淋巴细胞毒性抗风湿药物治疗,可能需要在T细胞收集期间继续治疗,并在CAR -T细胞输注后恢复治疗。因此,与没有自身免疫性疾病的人群相比,自体CAR -T细胞治疗是否会导致疗效受损或毒性差异,目前尚不清楚。但另一方面,鉴于B细胞在各种自身免疫性疾病的发展中起着至关重要的作用,患者可能会通过B细胞消耗来获得控制自身免疫性疾病的额外益处。
由于合并B-NHL和自身免疫性疾病的患者罕见,关于CAR -T细胞治疗的毒性和疗效的数据也非常有限,因此迫切需要研究CAR -T细胞疗法在这一人群中的应用。塞德曼癌症中心(Seidman Cancer Center) Jiasheng Wang教授牵头一项回顾性研究,利用大型汇总电子健康记录(EHR)数据库中接受同时商业化CD19 CAR-T细胞疗法的B-NHL伴风湿性自身免疫性疾病患者,并将毒性和结果与倾向性评分匹配的患者进行了比较,研究结果近日发表于《Bone Marrow Transplantation》。

研究结果
纳入数据库中接受商业化Axicabtagene ciloleucel (axi-cel)、tisagenlecleucel (tisa-cel)、lisocabtagene maraleucel (liso-cel)或brexucabtagene autoleucel (brexu-cel)的B-NHL伴风湿性自身免疫性疾病患者,风湿性自身免疫性疾病包括零碎性红斑狼疮(SLE)、类风湿性关节炎(RA)、干燥综合征、风湿性多肌痛(PMR)、强直性脊柱炎(AS)或牛皮癣,纳入“自身免疫性队列”。并进行1:1倾向性评分匹配,基线因素包括年龄、性别、种族、淋巴瘤类型、CAR - t细胞产物、既往治疗线、ECOG表现状态(ECOG PS)、乳酸脱氢酶(LDH)水平和血小板计数,应用于数据库中没有诊断出上述风湿性自身免疫性疾病的患者,称为“非自身免疫性队列”
基线特征
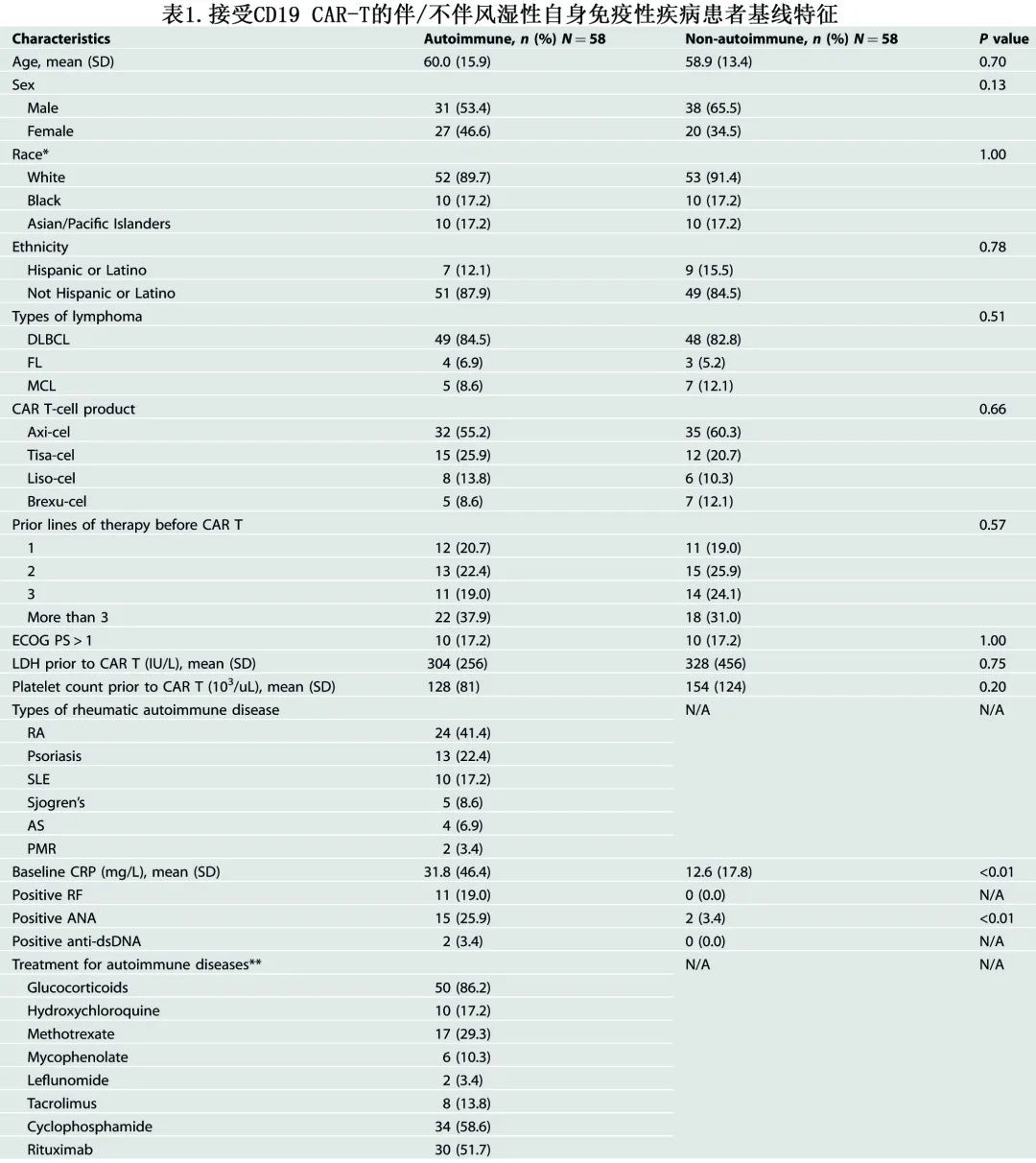
纳入58例,其中DLBCL是最常见亚型。基线时11例(19.0%)患者类风湿因子(RF)阳性,15例(25.9%)患者抗核抗体(ANA)阳性。大多数患者在基线时服用抗风湿疾病缓解药物(DMARD),包括羟氯喹(17.2%)、甲氨蝶呤(29.3%)、他克莫司(13.8%)和霉酚酸酯(10.3%)。
在倾向评分与人口统计学和与CAR - T相关毒性相关的已知因素(包括基线LDH和血小板计数)匹配后,自身免疫组和非自身免疫组各58例患者(表1)。
毒性及治疗
基于ASTCT CRS和ICANS分级系统,2021年引入CRS新编码,2022年引入ICANS新编码。在2021年1月后接受CAR-T细胞输注的30例自身免疫组患者和30例非自身免疫组患者中,任何级别的CRS(19[63.3%] vs 16 [53.3%],p=0.43)或高级别CRS(≥3级,3[10.0%] vs 2 [6.7%],p=0.63)均无显著差异(表2)。对于两组在2022年1月之后接受CAR-T细胞输注的17例匹配患者,任何级别(6[35.3%] vs 6[35.3%], p=1.00)或高级别(≥3级,2[11.8%]vs 1[5.9%], p=0.55)的ICANS均无显著差异。在两组58例匹配的患者中,炎症标志物铁蛋白和C反应蛋白(CRP)的峰值水平在第一周内相似(铁蛋白峰值平均值[±SD]为2466[±7438] vs 2862[±8329]ng/mL,p=0.57;CRP峰值平均值(±SD)为15.0(±28.7)和9.6±17.0 mg/L,p=0.32)。两组在铁蛋白、绝对中性粒细胞计数(ANC)和血小板计数方面也表现出相似的趋势。
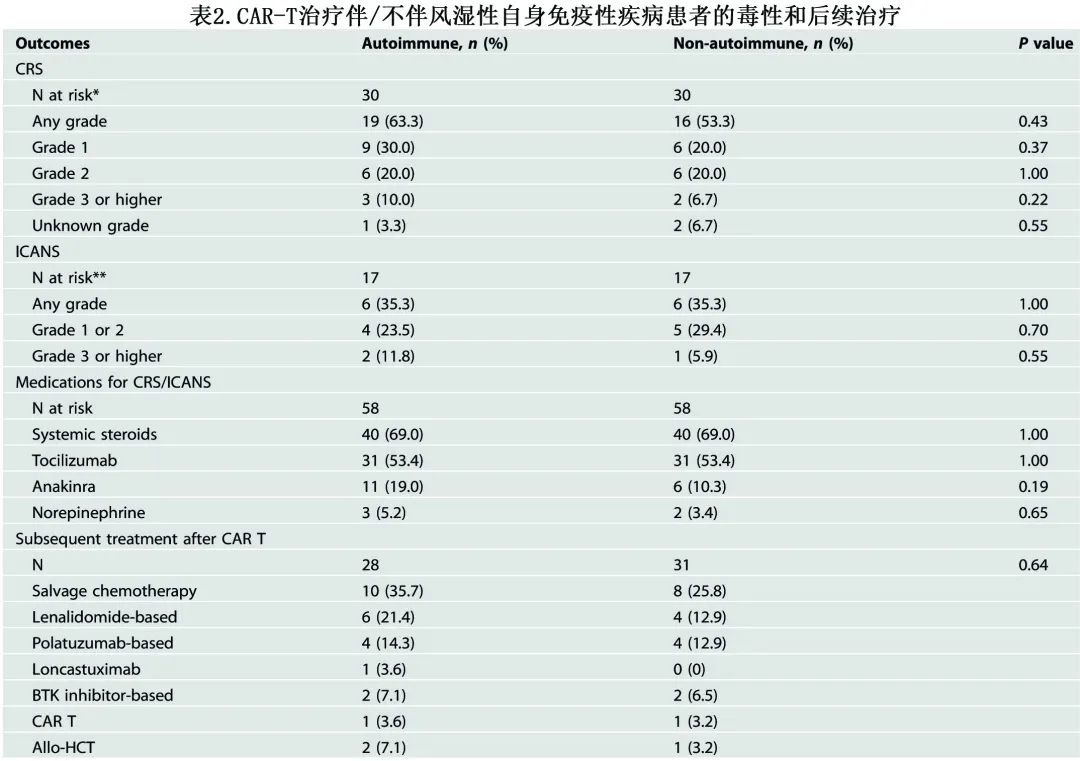
在治疗方面,两组患者使用系统性类固醇、托珠单抗、anakinra和去甲肾上腺素的情况相似(表2)。自身免疫组和非自身免疫组分别有5例(8.6%)和3例(5.2%)患者接受了ICU级别的护理。
生存结局和后续治疗
CAR-T细胞输注后第30天,自身免疫组和非自身免疫组的LDH水平无显著差异(平均[±SD], 289[±130.0] vs 339 [258.6] ng/mL,p=0.33)。中位随访328天和280天,自身免疫组和非自身免疫组至后线治疗或死亡(TNT-D)的中位时间分别为105天和162天,差异无统计学意义(风险比[HR]=0.97,p=0.91)。伴和不伴风湿性自身免疫性疾病的患者100天死亡率分别为10.3%和12.1%,此外两组的OS也相似(HR=0.90,p=0.76)(图1)。
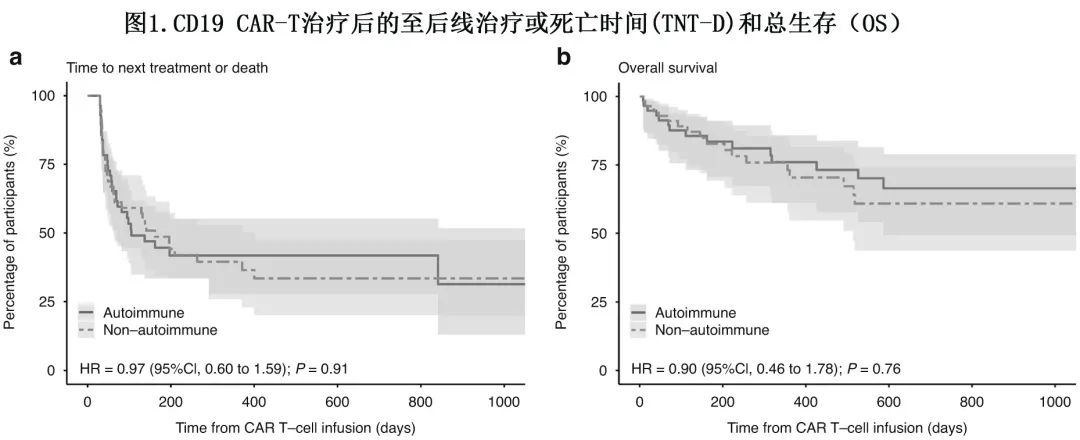
在单变量和多变量模型中研究了可能与OS相关的变量。在多变量分析中,仅诊断为DLBCL和基线LDH升高与较差的OS显著相关,风险比分别为1.57和2.39;而风湿性自身免疫性疾病的诊断与OS无显著相关性(HR=0.85)。
自身免疫组和非自身免疫组分别有28例(48.3%)和31例(53.4%)患者接受了后续抗癌治疗;无显著差异(p=0.64,log-rank检验)(表2);两组最常见的后续治疗为挽救性化疗(分别为35.7%和25.8%)。
风湿性自身免疫性疾病的结局
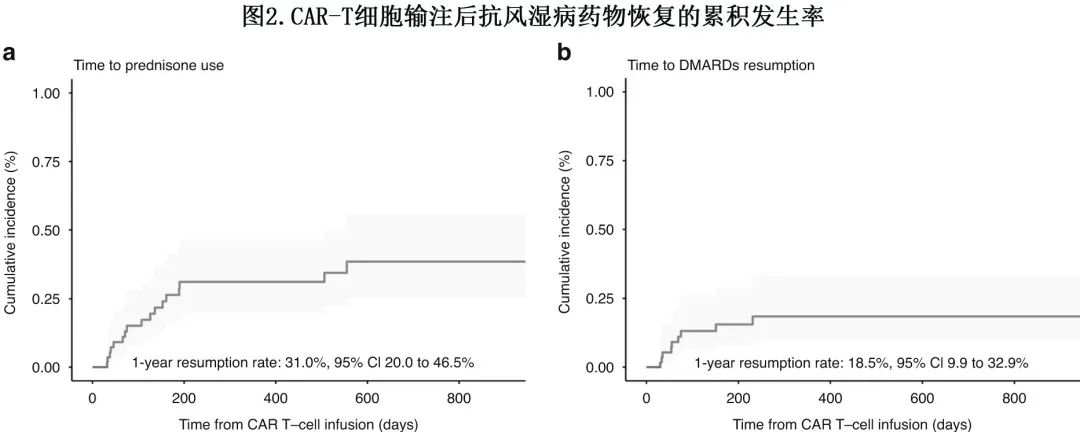
CAR-T细胞输注6个月后,CRP水平与基线相比显著降低(平均[±SD],12.6[±23.8] vs 31.8[±46.4]mg/L,p=0.03)。在第一年的自身抗体方面,5例患者仍为ANA阳性,1例患者为RF阳性,无患者为抗dsDNA阳性。第一年内13例(31.0%)患者接受了强的松治疗,1例和4例患者分别重新开始使用羟氯喹和甲氨蝶呤。强的松和DMARD恢复用药的累积发生率如图2所示。
总结
该回顾性研究使用电子数据库,比较了倾向性评分匹配的接受CD19 CAR-T细胞治疗的风湿性自身免疫性疾病患者和非风湿性自身免疫性疾病患者,发现在疗效或安全性方面没有显著差异:CRS和ICANS的发生率、严重程度和治疗相似,至后线治疗时间或死亡时间相似(HR=0.97,p=0.91),总生存率也也无差异(HR=0.90,p=0.76)。此外CAR-T细胞输注后自身免疫性疾病的生化控制得到改善,表现为炎症标志物降低、自身抗体血清阴性转化及类固醇和DMARD的使用减少。
总的来说,CAR-T细胞疗法在风湿性自身免疫性疾病患者中的安全性和有效性不受影响,此外还对风湿病取得了更好的生化控制。
参考文献
Wang JS,et al. CD19-targeted chimeric antigen receptor T-cell therapy in patients with concurrent B-cell Non-Hodgkin lymphoma and rheumatic autoimmune diseases: a propensity score matching study.Bone Marrow Transplant . 2023 Aug 21. doi: 10.1038/s41409-023-02086-1.


