J Thorac Oncol | 帕博利珠单抗 vs 必特芙普α治疗初治PD-L1高表达晚期非小细胞肺癌
时间:2023-08-24 13:42:24 热度:37.1℃ 作者:网络
非小细胞肺癌(NSCLC)约占所有肺癌的85%,是全球癌症死亡的主要原因,占2020年癌症死亡总数的18%。帕博利珠单抗是一种靶向程序性死亡1(PD-1)的单克隆抗体,是程序性死亡配体1(PD-L1)阳性(≥1%)晚期NSCLC患者一线治疗的标准。根据3期KEYNOTE-024试验,在PD-L1肿瘤比例评分(TPS)≥50%的患者中获得批准,与化疗相比,帕博利珠单抗改善了中位无进展生存期(PFS(10.3比6.0个月)和客观缓解率(ORR;45%比28%)。
在一项最新分析中,经过5年的随访,帕博利珠单抗的中位OS为26.3个月(95%CI:18.3-40.4),而化疗的中位OS为13.4个月(95%CI:9.4-18.3)(风险比[HR],0.62;95%CI:0.48-0.81)。根据KEYNOTE-042研究的结果,美国食品药品监督管理局的批准后来扩大到包括PD-L1 TPS≥1%的患者。除KEYNOTE-024和KEYNOTE-042外,其他几项3期研究还评估了免疫检查点抑制剂在PD-L1高表达晚期NSCLC患者中的使用,例如阿替利珠单抗(IMpower110),和西米普利单抗(EMPOWER Lung 1)。在这些研究中,PD-L1 TPS≥50%的患者,帕博利珠单抗的中位OS为20.0个月,阿替利珠单抗为20.2个月,西米普利单抗为NR;中位PFS范围为7.1-8.2个月,帕博利珠单抗和西米普利单抗的ORR均为39%。
尽管在晚期非小细胞肺癌患者中引入免疫检查点抑制剂后治疗结果有所改善,但由于许多患者对抗PD-(L)1疗法产生耐药性,该人群对有效治疗的需求仍未得到满足。转化生长因子β(TGF-β)在NSCLC组织中表达,与肿瘤进展,转移和抗癌治疗的耐药性有关。由于免疫监视受到抑制,TGF-β在癌症中的过度表达与肿瘤微环境中的转移有关,由于肿瘤微环境中T细胞浸润的限制,TGF-β表达的增加可能导致对PD-L1阻断反应的缺乏,因此结合免疫检查点抑制和TGF-β信号传导的阻断可能是一种有前途的治疗策略。
必特芙普α(Bintrafusp alfa)是一种一流的双功能融合蛋白,由人TGF-β受体II(TGF-βRII或TGF-β“trap”)的细胞外结构域组成。临床前数据表明,必特芙普α可以同时抑制PD-L1和TGF-β途径。一项使用必特芙普α 1200 mg进行二线治疗的1期研究表明,必特芙普α具有可控的安全性,并且在一部分PD-L1高表达的晚期NSCLC患者中显示出有希望的临床活性,PD-L1高表达的患者的确诊ORR为85.7%(PD-L1阳性[≥1%]患者的ORR为37.0%)。PD-L1阳性和PD-L1高表达患者的中位PFS分别为9.5个月和15.2个月;中位随访51.9周后,两组人群的中位OS均为NR。中位反应持续时间(由独立审查委员会(IRC)评估)为NR。
基于这些结果,该研究进行了这项3期试验,比较了必特芙普α和帕博利珠单抗在晚期NSCLC和高PD-L1表达患者的一线治疗中的作用。

方法:该项3期临床试验(NCT03631706)比较了必特芙普α与帕博利珠单抗作为PD-L1高表达晚期非小细胞肺癌患者一线治疗的疗效和安全性。主要终点是独立审查委员会(IRC)根据RECIST 1.1评估的总生存期(OS)和无进展生存期(PFS)。
结果:患者(N=304)以1:1的比例随机接受必特芙普α或帕博利珠单抗(每组N=152)。必特芙普α的中位随访时间为14.3个月(95%可信区间13.1-16.0个月),帕博利珠单抗的中位随访时间为14.5个月(95%可信区间13.1-15.9个月)。IRC评估的PFS在必特芙普α和帕博利珠单抗组之间没有显著差异(中位数7.0个月[95%Cl 4.2个月-未达到(NR)]与11.1个月[95%Cl 8.1个月-NR]);HR=1.232[95%CI,0.885-1.714])。必特芙普α的中位OS为21.1个月(95%CI 21.1个月-NR),帕博利珠单抗为22.1个月(95%CI:20.4个月-NR)(HR=1.201[95%CI,0.796-1.811])。必特芙普α与帕博利珠单抗相比,治疗相关不良事件(TRAE)更高;3/4级TRAE发生率分别为42.4%和13.2%。该研究在中期分析中停止,因为它不太可能达到主要终点。
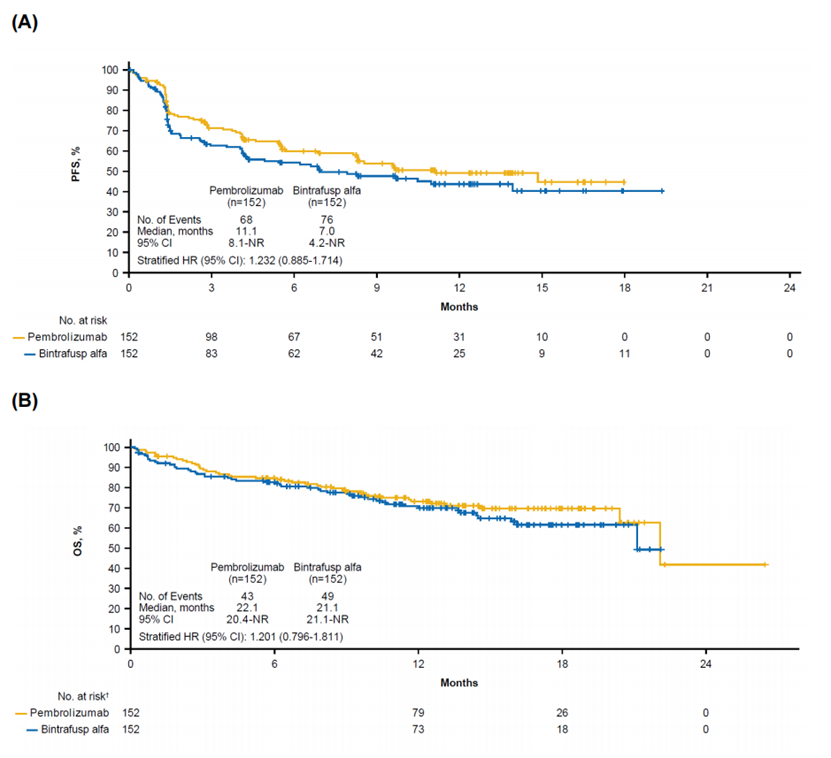
结论:与帕博利珠单抗相比,必特芙普α一线治疗PD-L1高表达晚期非小细胞肺癌患者的疗效并不优越。
原始出处:
Cho BC, et al. 2023. Bintrafusp alfa versus pembrolizumab in patients with treatment-naive, PD-L1–high advanced non-small cell lung cancer: a randomized, open-label, phase 3 trial. Journal of Thoracic Oncology.DOI: 10.1016/j.jtho.2023.08.018.


